Плоскодетекторная компьютерная томография в интервенционной радиологии: фундаментальные принципы, современные технологии и перспективы дальнейшего развития
Резюме
Создание в 2004 году ангиографических комплексов с возможностью выполнения плоскодетекторной компьютерной томографии (ПДКТ) и дальнейшее развитие ПДКТ-технологий произвело революцию в возможностях визуализации, планирования, навигации, слежения, мониторинга и оценки непосредственного ответа на лечение в различных направлениях интервенционной радиологии (рентгенохирургии). Современный ангиографический комплекс, оснащенный ПДКТ (ПДКТ на С-дуге), является единственной системой лучевой визуализации, позволяющей в одной рентгеноперационной и на одном операционном столе выполнять как рентгеноскопию, рентгенографию, ангиографию, цифровую субтракционную ангиографию, так и компьютерную томографию при проведении различных эндоваскулярных, чрескожных, внутрипросветных и комбинированных вмешательств в едином стереотаксическом пространстве и 3D-режиме реального времени. За относительно короткий период времени ПДКТ на С-дуге из мало кому известного метода лучевой визуализации превратилась в мощный комплекс различных визуализационных и навигационных технологических решений, позволивших значительно повысить безопасность и улучшить непосредственные и отдаленные результаты лечения пациентов с многими сердечно-сосудистыми, онкологическими и другими заболеваниями. С другой стороны, стремительное развитие ПДКТ привело к разрыву в знаниях между доступными для использования ПДКТ-технологиями, интегрированными в современные ангиографические комплексы, и осведомлённостью об этих технологиях практикующих врачей отделений рентгенохирургических методов диагностики и лечения. Цель статьи – кратко описать фундаментальные принципы работы ПДКТ на С-дуге, современные ПДКТ-технологии, доступные для клинического использования, а также перспективы их дальнейшего развития.
Введение
Плоскодетекторная компьютерная томография (ПДКТ) – это метод рентгеновской компьютерной визуализации, в котором для получения объемных и кроссекционных изображений используется рентгеновский пучок пирамидальной формы, проецируемый на прямоугольную или квадратную матрицу твердотельного плоского детектора в режиме ротационной рентгенографии. В настоящее время ПДКТ широко используется в различных специализированных диагностических ПДКТ-сканерах (прежде всего в челюстно-лицевых и ортопедических компьютерных томографах, компьютерных томографах для молочных желез и т.д.), применяется для визуализации и навигации в травматологии, ортопедии и нейрохирургии (благодаря ее интеграции в O-arm системы), а также входит в состав линейных ускорителей для планирования и мониторинга лучевой терапии [1]. Однако, наибольшее развитие технологии ПДКТ получили в области интервенционной радиологии благодаря их удачной интеграции в многофункциональные ангиографические комплексы.
Первые ангиографические установки с возможностью выполнения ПДКТ (ПДКТ на С-дуге) были выпущены на рынок в 2004 г. [2]. При проектировании ПДКТ на С-дуге производители оборудования старались соблюдать определенный компромисс между качеством КТ-визуализации, скоростью реконструкции изображений, разумной лучевой нагрузкой и простотой использования аппаратуры в рентгеноперационных. В начале своего клинического использования ПДКТ на С-дуге позиционировалась производителями только как «полезная опция», позволяющая получать изображения «достаточного для проведения лечебных вмешательств качества» и полностью полагающаяся на данные «классических технологий лучевой визуализации», таких как МСКТ, МРТ, ПЭТ-КТ и др. [3, 4].
Однако, в дальнейшем стало очевидно, что благодаря очень высокому пространственному разрешению и возможности селективного внутриартериального (и других видов) контрастирования ПДКТ на С-дуге имеет очевидные преимущества как самостоятельный метод диагностики, в частности для визуализации оккультных интракраниальных аневризм, а также оценки артериальной и венозной анатомии головного мозга [5-7]. По мере дальнейшего развития ПДКТ происходила модернизация как самих плоских детекторов, так и программного обеспечения, и вычислительных мощностей, а данные клинических исследований продолжали демонстрировать очевидные преимущества ПДКТ не только для диагностики, но и для эффективного лечения многих заболеваний. Так, в 2010 г. J. Iwazawa et al. показали, что ПДКТ в артериальную фазу артериогепатикографии (ПДКТ-артериогепатикография) обладает в два раза большей чувствительностью по сравнению с многофазной МСКТ на фоне внутривенного контрастирования для диагностики узлов гепатоцеллюлярного рака (ГЦР) диаметром менее 10 мм [8]. В том же 2010 году П.В. Балахнин с соавт. представили принципиально новый метод визуализации метастазов колоректального рака в печени, основанный на выполнении ПДКТ в капиллярную фазу инфузионной артериогепатикографии (введение контрастного препарата в общую печеночную артерию в течение 20 с, начало ПДКТ-сканирования на 22 с) [9]. Этот метод продемонстрировал значительно большую чувствительность и специфичность по сравнению с многофазной МСКТ на фоне внутривенного контрастирования для диагностики метастазов колоректального рака в печени диаметром менее 20 мм и, в особенности, – диаметром менее 10 мм [10, 11].
Становление и развитие лечебных технологий ПДКТ на С-дуге неразрывно связано с появлением и внедрением двух принципиально новых технологий чрескожной и внутрисосудистой навигации, основанных на объединении (слиянии) трехмерной ПДКТ-визуализации с двумерной рентгеноскопией, – так называемых технологий дополненной реальности или дополненной рентгеноскопии. В 2007 г. J.M. Racadio et al. впервые сообщили об успешном использовании технологии чрескожной (стереотаксической) навигации в режиме реального времени при проведении различных интервенционно-радиологических вмешательств [12]. Используя уникальные возможности ПДКТ-визуализации и чрескожной ПДКТ-навигации M. Morimoto et al. уже в 2010 г. разработали методику ангиографически-ассистированной чрескожной микроволновой абляции (МВА) гиперваскулярных узлов ГЦР [13], а П.В. Балахнин с соавт. в 2018 – методику ангиографически-ассистированной чрескожной криоабляции метастазов колоректального рака в печени под ПДКТ-контролем [14, 15]. Высокая эффективность ангиографически-ассистированной чрескожной термоабляции (МВА и криоабляции) под ПДКТ-контролем в дальнейшем была подтверждена и другими исследователями, сделавшими вывод о том, что данный метод может стать стандартом чрескожной локальной терапии первичных и метастатических опухолей печени в ближайшем будущем [16, 17]. В настоящее время чрескожная стереотаксическая навигация в режиме дополненной рентгеноскопии (реального времени) широко используется при проведении большого числа как диагностических (например, чрескожная стереотаксическая биопсия опухолей легких), так и лечебных (например, чрескожная эмболизация мест утечек лимфы) интервенционно-радиологических процедур [18].
В 2010 г. F. Deschamps et al. впервые представили технологии определения питающих опухоль сосудов и внутрисосудистой стереотаксической навигации в режиме реального времени (режиме дополненной рентгеноскопии) предназначенные для проведения суперселективной катетеризации и суперселективной трансартериальной химиоэмболизации (ссТАХЭ) узлов ГЦР [19]. Использование этих технологий принципиальным образом повысило точность выявления питающих узлы ГЦР артерий, скорость их катетеризации, равномерность эмболизации и, как следствие эффективность ссТАХЭ, что было подтверждено рядом крупных исследований [20, 21]. В метаанализе 2024 г. было убедительно показано, что использование этих технологий привело к трехкратному увеличению общей трехлетней выживаемости пациентов, страдающих ГЦР, по сравнению с пациентами, получающими ссТАХЭ только под контролем цифровой субтракционной ангиографии (ЦСА) [22]. Аналогичные данные были продемонстрированы и в азиатских группах пациентов, получавших ссТАХЭ с использованием и без использования визуализационных и навигационных ПДКТ-технологий [23], а также в ряде отечественных исследований [24, 25]. В настоящее время технологии внутрисосудистой навигации и другие технологии слияния изображений и 3D-роадмаппинга широко используются также для эмболизации доброкачественных опухолей (например, для лечения доброкачественной гиперплазии предстательной железы), артериовенозных мальформаций, поиска артерий, являющихся источником кровотечения, установки стент-графтов, эмболизации эндоликов после стентирования и многих других целей [26].
Можно говорить о том, что внедрение ПДКТ на С-дуге произвело революцию в возможностях визуализации, планирования, навигации, слежения, мониторинга и оценки непосредственного ответа на лечение во всех направлениях интервенционной радиологии и прежде всего в интервенционной онкологии и интервенционной нейрорадиологии [27, 28]. Современный ангиографический комплекс, оснащенный ПДКТ, является единственной системой лучевой визуализации, позволяющей в одной рентгеноперационной и на одном операционном столе выполнять как рентгеноскопию, рентгенографию, ангиографию, ЦСА, так и компьютерную томографию при проведении различных эндоваскулярных, чрескожных, внутрипросветных и комбинированных вмешательств в едином стереотаксическом пространстве и 3D-режиме реального времени [29]. За относительно короткий период времени ПДКТ на С-дуге из мало кому известного метода лучевой визуализации превратилась в мощный комплекс различных визуализационных и навигационных технологических решений, позволивших значительно повысить безопасность и улучшить непосредственные и отдаленные результаты лечения пациентов с многими сердечно-сосудистыми, онкологическими и другими заболеваниями [30, 31].
В 2024 г. Китайская коллегия интервенционных радиологов опубликовала консенсус, который настоятельно рекомендует использовать ПДКТ-визуализацию в комбинации с технологиями внутрисосудистой и чрескожной навигации практически на всех этапах проведения процедур ссТАХЭ и чрескожной термоабляции при лечении ранних и промежуточных стадий ГЦР [32]. В нашей стране использование ПДКТ также рекомендовано при проведении локорегионарной терапии этого заболевания [33, 34]. Очевидно, что в будущем потребность в использовании ПДКТ-визуализации и высокоэффективных ПДКТ-технологий будет только увеличиваться. В связи с этим понимание фундаментальных принципов работы ПДКТ, особенностей реконструкции и использования кроссекционных изображений, принципов и алгоритмов реализации различных программных пакетов, а также информированность о получаемых пациентом и персоналом дозах ионизирующего излучения становятся совершенно необходимыми для врачей, работающих в различных направлениях интервенционной радиологии. В то же время в России наблюдается существенный разрыв в знаниях между доступными для использования ПДКТ-технологиями, интегрированными в современные ангиографические комплексы, и осведомленностью об этих технологиях практикующих врачей отделений рентгенохирургических методов диагностики и лечения. Связано это с тем, что систематическое обучение профильных специалистов использованию ПДКТ в нашей стране не проводится, а учебная и справочная литература на русском языке практически полностью отсутствует. Цель статьи – кратко описать фундаментальные принципы работы ПДКТ на С-дуге, современные ПДКТ-технологии, доступные для клинического использования, а также перспективы их дальнейшего развития.
Фундаментальные принципы работы ПДКТ на С-дуге
1. Конструкция плоских детекторов
Подробно история создания первых ангиографических систем, оснащенных технологией ПДКТ, равно как и особенности использования рентгеновских пучков веерной, конической и пирамидальной формы при проведении рентгеновской компьютерной томографии были рассмотрены нами ранее в другой работе [2]. Здесь же следует отметить, что практически во всех современных ангиографических комплексах в настоящее время используются плоские цифровые детекторы первого поколения, представляющие собой двухслойные твердотельные плоские панели с непрямым (двухуровневым) процессом преобразования рентгеновских лучей в электрический сигнал [35]. Первый сцинтилляционный слой панели состоит из тонких (диаметром 5–10 мкм) игольчатых конусовидных кристаллов йодида цезия легированного таллием (CsI:Tl), преобразующих проходящие через них рентгеновские кванты в свет. Структура кристаллов в форме игл действует как световой направитель, благодаря чему сфокусированный свет точно попадет на расположенную под каждым кристаллом ячейку, содержащую слой аморфного гидрированного кремния (a-Si:H), являющегося микроскопическим фотокатодом, генерирующим электрический сигнал. При том, что фотокатод занимает только 60–70% площади каждой ячейки (пикселя), поглощение рентгеновского излучения со средней энергией 53 кэВ дает возможность генерировать электрический сигнал, состоящий из 800–1000 электронов [36]. Каждый фотокатод, в свою очередь непосредственно связан с тонкопленочным транзистором (thin-film transistor, TFT), усиливающим электрический сигнал и передающим его (как сигнал от дискретного пикселя) для последующей обработки в компьютер [37].
Применяемый в настоящее время для производства детекторов на основе a-Si:H и CsI:Tl (a-Si:H/CsI:Tl) метод плазменного осаждения позволяет создавать активные рабочие матрицы размерами 40х30 см и даже 41х41 см, состоящие из нескольких миллионов пикселей размером от 154 до 200 мкм (в зависимости от производителя) каждый. Поэтому эти детекторы оказались подходящими для использования в области интервенционной нейрорадиологии и интервенционной онкологии, где требуется сканирование больших областей, таких как голова, легкие или печень [2]. Как было показано в ряде исследований, увеличение толщины кристаллов CsI:Tl более 200 мкм улучшает квантовую эффективность детектора за счет более полного поглощения энергии, что повышает его чувствительность. Но это, к сожалению, резко уменьшает пространственное разрешение из-за оптической диффузии размытия [35-37]. Плоские детекторы a-Si:H/CsI:Tl имеют достаточно высокое контрастное разрешение и большой динамический диапазон, позволяющий в настоящее время проводить ротационную рентгенографию с получением ПДКТ-данных от каждого пикселя матрицы с частотой 7,5 кадров в сек. В то же время существенным недостатком a-Si:H является относительно медленная скорость разряда транзисторных элементов, а это приводит к тому, что некоторая часть сигнала, накопленная в одном кадре может быть считана в последующих кадрах, обуславливая тем самым так называемый эффект временного запаздывания. Еще одной причиной запаздывания считается послесвечение CsI:Tl, однако это влияет на работу детектора в значительно меньшей степени. Кроме того, все еще существуют проблемы со скоростью передачи информации от каждого пикселя в компьютер, а также с вычислительными мощностями самих компьютеров ангиографических установок, что также замедляет общую работу системы. Поскольку сканирование должно быть максимально быстрым, а скорость реконструкции изображений в интервенционной радиологии не должна превышать нескольких секунд (в отличие от диагностических систем, практически не ограниченных временем реконструкции) для оперативного получения 3D-изображений в большинстве случаев приходится жертвовать другими параметрами визуализации. В частности, для повышения контрастного разрешения необходимо получение как можно большего числа проекционных изображений для чего требуется увеличение скорости рентгеновской съемки до 30 и даже 60 кадров в секунду. (для сохранения приемлемого времени сканирования). В связи с ограничениями пропускной способности каналов передачи данных, не позволяющих в настоящее время передавать сигнал от всех пикселей с такой частотой кадров, при увеличении скорости съемки требуется объединение нескольких соседних пикселей в один в режиме 2х2 пикселя или 4х4 пикселя (режим биннинга пикселей). Это в свою очередь, прогрессивно снижает пространственное разрешение ПДКТ. Таким образом конструкция используемых в настоящее время плоских детекторов на основе a-Si:H/CsI:Tl является компромиссом между необходимым полем обзора (field of view, FOV), а также пространственным, контрастным и временным разрешением с преимущественным акцентом на пространственное разрешение при эквивалентной излучаемой дозе [3, 4, 35-37]. Необходимо отметить, что все производители постоянно осуществляют «доработку» плоских детекторов на основе a-Si:H/CsI:Tl, увеличивая пропускную способность кабелей и глубину обработки данных, что приводит к постепенному улучшению качества получаемых изображений.
Так, одним из первых плоских детекторов, широко использовавшихся в ангиографических установках в 2000-е гг. был детектор Pixium 4700 производства компании Trixell (Муаран, Франция), состоящий из 2480×1910 пикселей с шагом в 154 мкм, активной матрицей размерами 382×294 мм, 14-битным аналогово-цифровым преобразователем (АЦП) и кадровой частотой 7,5 кадров в секунду при биннинге 1х1 и 30 кадров в секунду при биннинге 2×2. Интегрированный в ангиографическую установку Artis zee (Siemens Healthineers, Германия) данный плоский детектор (коммерческое обозначение - as40) обладал квантовой эффективностью 73%, серошкальным диапазоном в 16384 оттенков серого и пространственным разрешением 3,25 lp/mm (lines per millimeter, линий на миллиметр), достаточным для визуализации сосудов диаметром до 0,3 мм [35]. Модернизированный несколько лет спустя детектор той же компании, получивший название Pixium 3040CV, был оснащен уже 16-битным АЦП и улучшенной схемой считывания, благодаря чему обладал квантовой эффективностью 77%, серошкальным диапазоном в 65536 оттенков серого (в 4 раза выше, чем в первой модели) и улучшенным соотношением сигнал шум при пространственном разрешении в 2,9 lp/mm. Использование этого обновленного детектора с расширенным динамическим диапазоном (под коммерческим обозначением as40HDR) компанией Siemens Healthineers (Германия) в ангиографических установках Artis Q, а позднее и в Artis zee сразу существенно улучшило визуализацию мягких тканей при низких контрастах и расширило клинические возможности ПДКТ для качественной визуализации низкоконтрастных структур, в первую очередь таких как паренхима головного мозга и паренхима печени [35].
2. Пространственное разрешение
Высокое пространственное разрешение является ключевой сильной стороной ПДКТ, благодаря которой достигается четкая визуализация сосудов диаметром 250–300 мкм (0,25-0,30 мм) при проведении ПДКТ-артериографии (рис. 1). Такое высокое разрешение ПДКТ позволяет осуществлять прецизионный 3D-контроль установки стентов, микрокатетеров, тонких пункционных игл и других устройств непосредственно в рентгеноперационной (рис. 2). Пространственное разрешение характеризует точность воспроизведения малых структур в изоцентре и зависит от ряда факторов, таких как шаг пикселя, площадь сцинтиллятора, размер фокального пятна, геометрическое увеличение, стабильность системы во время сканирования, а также используемых фильтров реконструкции. Как уже было отмечено, применяемые в настоящее время a-Si:H/CsI:Tl ПДКТ-детекторы имеют высокие частотно-контрастные характеристики, благодаря конусовидному направлению света к каждому фотодиоду. Более толстый слой CsI улучшает поглощение, но увеличивает боковое размытие, снижающее контрастность, поэтому толщина и размер пикселя оптимизируются совместно [3, 4]. Пространственное разрешение напрямую зависит от режима считывания данных: при объединении (биннинге) пикселей, направленном на снижение шума и повышение контрастности получаемых изображений, пространственное разрешение прогрессивно снижается [35]. Как было показано в исследованиях на фантомах, ангиографическая установка Artis zee (Siemens Healthineers, Германия) при функции передачи модуляции (modulation transfer functions, MTF) в 10% достигает пространственного разрешения в 3,0 lp/mm при нативном считывании (1×1) и 1,5 lp/mm при биннинге 2×2, что превосходит разрешающую способность МСКТ (1,2–1,4 lp/mm в режимах высокого разрешения) [1, 35]. При использовании всех пикселей без их объединения разрешение может достигать почти 4,0 lp/mm, что соответствует возможности распознавания высококонтрастных деталей толщиной 130 мкм (0,13 мм) [35]. Переход на биннинг 2×2 удваивает размер эффективного пикселя с 154 мкм до 308 мкм, снижая MTF 10% вдвое, но повышая кадровую частоту до 30 кадров в секунду и минимизируя шум. При биннинге 4×4 (размер эффективного пикселя 616 мкм) разрешение падает до 1,0 lp/mm, однако возросшая скорость съёмки (60 кадров в секунду) и большее число проекций сокращает артефакты движения и улучшает контрастное разрешение, что чаще всего используется при визуализации органов брюшной полости и малого таза [35].
Рис. 1 (а-г). Церебральная ПДКТ-артериография бассейна правой общей сонной артерии, демонстрирующая возможность визуализации артерий диаметром 0,5 мм
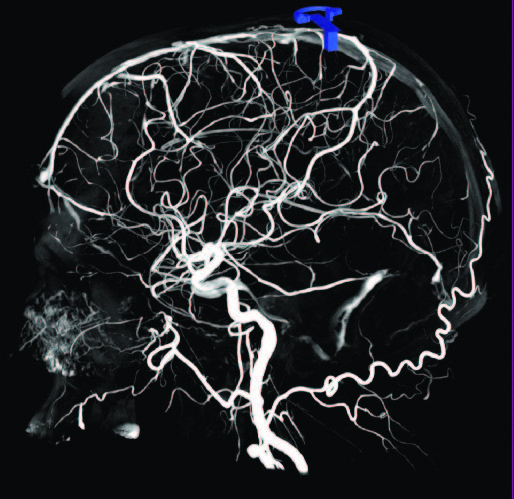
Рис. 1а. Реконструкция всего артериального русла после проведения ПДКТ в режиме 20sDCT Head (Siemens Healthineers, Германия) с введением 60 мл контрастного препарата со скоростью 2 мл/с (в течение 30 с) и задержкой сканирования 10 с
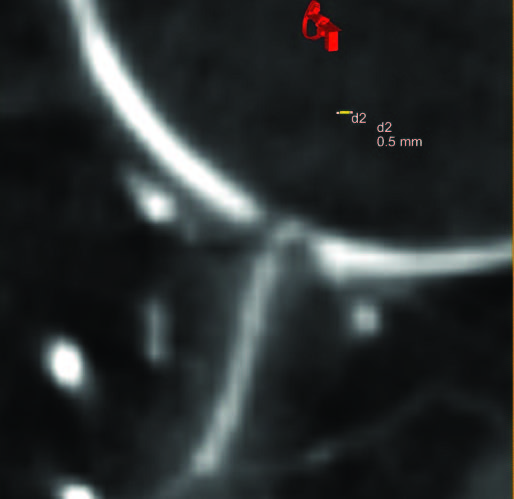
Рис. 1б. Визуализация правой центральной артерии сетчатки глаза диаметром 0,5 мм в режиме MIP (тонкие срезы) у того же пациента
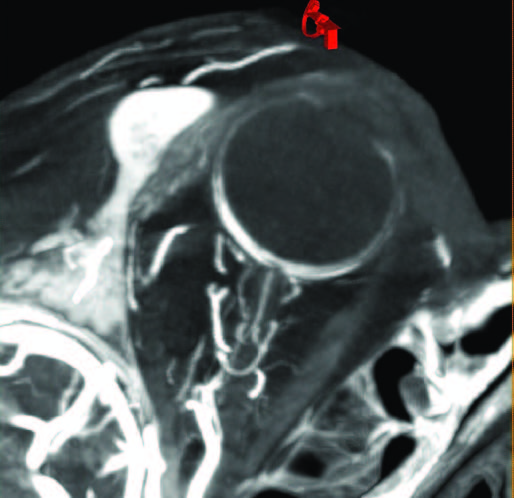
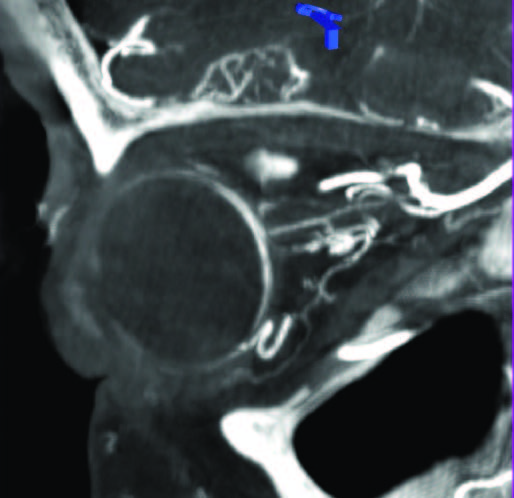
Рис. 1в-г. Визуализация той же артерии и дренирующих вен в косых проекциях (MIP) с использованием более толстых срезов.
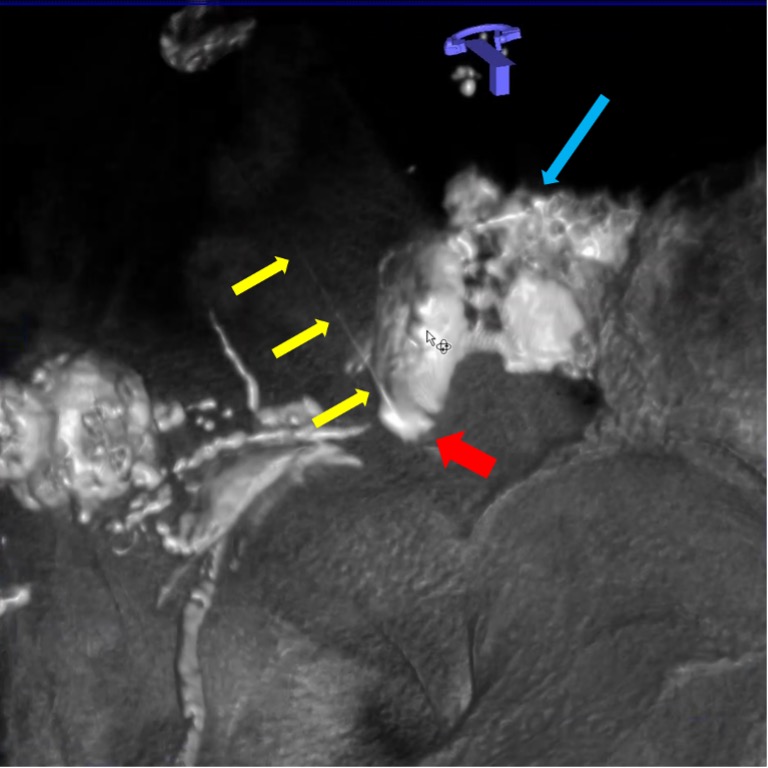
Рис. 2. Интранодальная паховая ПДКТ-лимфангиография с последующей чрескожной пункцией лимфопсевдоаневризмы (толстая красная стрелка) иглой 25 G (0,5 мм) (тонкие желтые стрелки) с целью эмболизации массивной послеоперационной тазовой лимфореи (длинная синяя стрелка): ПДКТ позволяет отчетливо визуализировать пункционную иглу на реконструированных изображениях и точно определить положение ее дистальной части.
Пространственное разрешение ПДКТ напрямую зависит от угла конического пучка и угловой выборки – при отдалении от центральной оси сканирования оно снижается за счет «дефицита данных», что по сути, является фундаментальной проблемой конических рентгеновских пучков в целом и ПДКТ на С-дуге, в частности (рис. 3). При этом выбор траектории сканирования и ядра реконструкции определяет, насколько хорошо высокочастотные детали сохраняются во всем объеме [37]. Модифицированные алгоритмы ротации системы «источник-детектор» (например, синусоидальная траектория сканирования) повышают однородность выборки и помогают сохранить высокую детализацию в трёхмерном объёме [38, 39] Любые движения во время сканирования в виде дыхания пациента, сокращений сердца, пульсации сосудов, дрожания С-дуги или стола, прогрессивно снижают частотно-контурную характеристику и приводят к резкому ухудшению качества визуализации [40, 41].
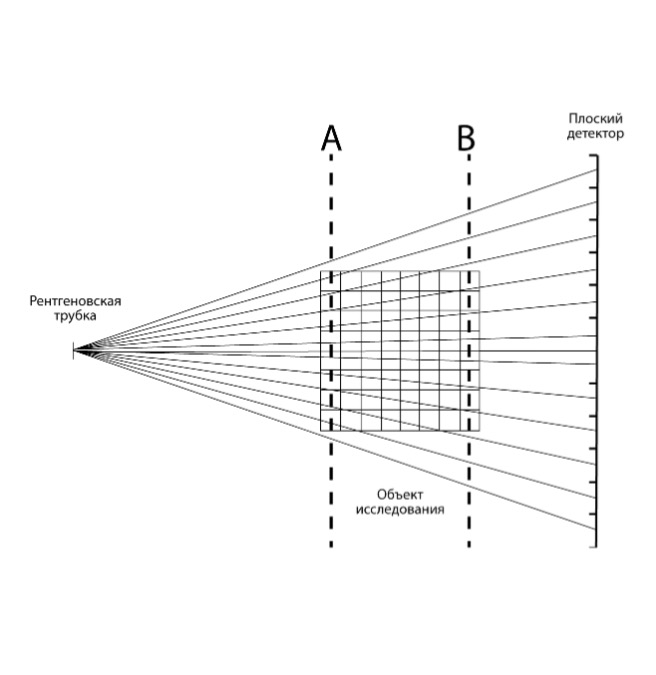
Рис. 3. Схематическая визуализация одной из основных причин недостаточной выборки данных при проведении сканирования с использованием пирамидальной формы излучения: проблема заключается в сильном расхождении лучей при их следовании от рентгеновской трубки к плоскому детектору; очевидно, что срез A, проходящий через объект исследования и располагающийся ближе всего к источнику, «собирает» гораздо больше «лучей на воксель» (измеряется на отдельных пикселях детектора), чем срез B, который находится ближе всего к детектору; таким образом общее количество «лучей на воксель» линейно уменьшается с удалением срезов от источника излучения (адаптировано из [51]).
Важной особенностью ПДКТ является то, что она не требует во время реконструкции изображений использования алгоритмов Z-интерполяции, необходимой при проведении МСКТ, использующей «спиральное» сканирование. В связи с этим реконструированный объем ПДКТ-данных является истинно волюметрическим, то есть состоящим из вокселей правильной формы в виде кубов (все стороны вокселя равны), а не прямоугольных параллелепипедов. Это позволяет с одинаково высоким разрешением просматривать реконструированные ПДКТ-изображения в любой плоскости, в то время как пространственное разрешение МСКТ-данных при просмотре в коронарных и сагиттальных проекциях может существенно отличаться в худшую сторону от пространственного разрешения на аксиальных «срезах» [3, 4, 37, 40].
3. Контрастное разрешение
Контрастное разрешение (low-contrast detectability, LCD) определяет минимальную разницу рентгеновской плотности (измеряемой в единицах Хаунсфилда, HU) при известном размере объекта, которую система способна надёжно различить на одном и том же уровне шума. При этом чем меньше объект, тем большая разность контрастирования необходима для его обнаружения. В практической работе это означает возможность или невозможность визуализации «свежих» кровоизлияний в паренхиме головного мозга, мелких гиповаскулярных метастазов в печени или зон абляции в почке после проведения локальной термодеструкции. Контрастное разрешение ПДКТ ограничивается главным образом высоким квантовым шумом и рассеянием рентгеновского излучения, которые ослабляют низкочастотный контраст и приводят к артефактам в виде «купола» и «полос». Эти артефакты реконструкции характерны также и для МСКТ, использующей пучки как веерной, так и пирамидальной формы, но при ПДКТ они выражены значительно сильнее из-за большего угла рентгеновского излучения и широкого поля обзора. В то время как МСКТ сканеры (256- и 320-срезовые) с успехом используют анти-рассеивающие решетки между отдельными рядами детекторов, что в значительной степени решает проблему квантового шума, анти-рассеивающие решетки для ПДКТ далеки от совершенства и значительно увеличивают дозу облучения [3, 4, 35-37]. В связи с этим соотношение рассеянного излучения к первичному на поверхности плоских детекторов может составлять 3,0 для ПДКТ по сравнению примерно с 0,2 для МСКТ, что и объясняет большую часть различий в контрастности изображений, наблюдаемых между двумя методами визуализации [3, 4, 35-37]. Рассеянная радиация, более низкая квантовая эффективность и более низкий динамический диапазон плоских детекторов из CsI являются причиной того, что контрастное разрешение ПДКТ на ранних этапах развития технологии (при сопоставимой или даже более низкой лучевой нагрузке) почти в два раза уступало контрастному разрешению МСКТ: разница затухания составила 5 HU/5 мм против 3 HU/5 мм, соответственно [3, 4, 35-37]. Эти особенности ПДКТ не влияют на качество визуализации высококонтрастных структур (артерии, содержащие контрастный препарат, трабекулярные структуры костей и т.д.), но их необходимо учитывать при разработке режимов контрастирования мягких тканей и паренхиматозных органов.
Дополнительно повысить контрастное разрешение мягких тканей путем улучшения соотношения контраст/шум (contrast noise ratio, CNR) возможно путем увеличения экспозиции рентгеновского излучения, приводящей к увеличению дозы, что в настоящее время считается нецелесообразным [42-45]. Более перспективным вариантом представляется использование для реконструкции изображений новых математических алгоритмов на основе искусственного интеллекта (ИИ) и глубокого машинного обучения, которые уже сегодня позволяют в значительно степени нивелировать разницу между контрастным разрешением ПДКТ и МСКТ при сопоставимой дозе облучения. В настоящее время ПДКТ в режиме «абдоминального» биннинга 4×4 позволяет со 100% вероятностью обнаруживать образования диаметром 5 мм с разницей контрастирования в 10 HU и диаметром 10 мм с разницей контрастирования в 5 HU, то есть достаточно мелкие структуры диаметром 10 мм всего на 0,5% отличающиеся по своей контрастности от фона [3, 4, 35-37]. Однако принципиальное улучшение контрастной визуализации ПДКТ в будущем, большинство исследователей связывает с созданием плоских панелей нового поколения, основанных на двухэнергетическом принципе сканирования или прямом фотонном считывании, что будет рассмотрено ниже.
4. Временное разрешение
Временное разрешение ПДКТ отражает, насколько хорошо система «замораживает» анатомические структуры во время ротационного сканирования. Оно определяется временем экспозиции на проекцию (шириной импульса), частотой и количеством проекций, а также общим временем вращения гентри. Эти параметры ограничены механикой С-дуги, свойствами детектора, соотношением дозы и квантового шума и числом необходимых для реконструкции проекций. Более высокая частота импульсов и проекций уменьшает размытость изображений при движении, но увеличивает уровень шума, поэтому современные протоколы сканирования обеспечивают баланс между высоким временным разрешением с одной стороны и качеством изображения и дозой с другой [3, 37, 42]. Основным условием получения качественной ПДКТ-визуализации является обеспечение максимально возможной неподвижности сканируемых структур, поэтому длительность сканирования имеет критически-важное значение: задержка дыхания пациентом в течение 3 с переносится значительно легче, чем задержка дыхания в течение 20 с. Временное разрешение играет ключевую роль при сканировании подвижных органов, таких как легкие или печень, так как неконтролируемое дыхание пациента является критическим фактором, ухудшающим качество визуализации за счет появления размытости и полос (рис. 4). Сердечные движения во время сканирования также снижают визуализацию низкоконтрастных деталей и именно этим объясняется худшая выявляемость опухолей печени, локализующихся во 2 и 3 сегментах печени, тесно прилежащих к сердцу. Необходимо отметить, что все производители непрерывно снижают длительность времени ПДКТ-ротации, за счет улучшения контрастного разрешения детекторов, оптимизации алгоритмов сканирования и реконструкции, а также расширения каналов передачи данных и скорости вычислений. Так, если в первой модели ангиографа Artis zee (Siemens Healthineers, Германия) сканирование головного мозга занимало 20 с, с получением 500 проекционных изображений, то уже в новой системе ARTIS icono (Siemens Healthineers, Германия) это время сокращено до 8 с с сохранением того же количества изображений и улучшенным качеством визуализации интракраниальных структур. Существенный вклад в ухудшение качества визуализации может вносить также пульсация артерий (рис. 5). Так как осуществлять ПДКТ-сканирование с субсекундной скоростью практически невозможно, для устранения подобных артефактов движения в настоящее время используются дополнительные алгоритмы реконструкции, получившие название алгоритмов «коррекции движения на основе модели» [46]. Альтернативой в будущем может стать использование 4D-биннинга (например, респираторной фазы), улучшающего временную точность за счет реконструкции подмножества проекций, получаемых без задержки или частичной задержки дыхания пациента, что будет обсуждено ниже.
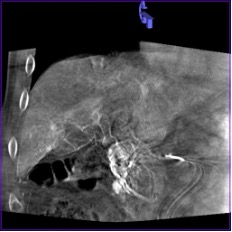
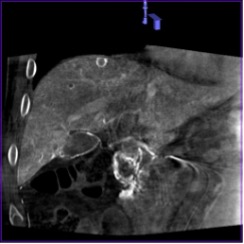
Рис. 4 (а, б). Пример, демонстрирующий выраженные артефакты движения, связанные с дыханием при проведении ПДКТ у пациента с подозрением на метастазы колоректального рака в печени: а. ПДКТ в капиллярную фазу артериогепатикографии (введение 40 мл контрастного препарата в общую печеночную артерию со скоростью 2 мл/с и начало сканирования на 22 с в режиме 6sDCTBody (Siemens Healthineers, Германия)) выполнено на фоне неглубокого вдоха – визуализируются множественные артефакты движения в виде полос и размытости контуров, метастазы в печени отчетливо не определяются; б. повторное ПДКТ-сканирование выполнено в том же режиме через три минуты после первого с полной задержкой дыхания пациентом (после проведения его дополнительного обучения) – в поддиафрагмальных отделах печени отчетливо визуализируется метастаз колоректального рака диаметром 9 мм с характерным перитуморальным контрастированием по периферии; артефакты движения в зоне интереса отсутствуют, однако сохраняются артефакты движения, связанные с пульсацией аорты (в виде размытости контуров ангиографического катетера).
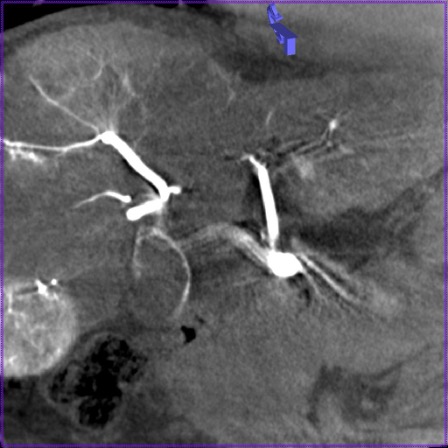
Рис. 5. Пример, демонстрирующий артефакты движения, связанные с пульсацией артерий и сердцебиением при проведении ПДКТ у пациента с гепатоцеллюлярным раком: наблюдаются выраженные артефакты движения в виде полос и размытости контуров левой печеночной артерии, связанные как пульсацией самой артерии, так и с движениями левой доли печени, обусловленными сокращениями сердца; визуализация правой печеночной артерии не изменена.
Вторым важным временным параметром является скорость реконструкции изображений, которая в отличие от диагностических исследований не должна превышать нескольких секунд. Рост производительности компьютеров уже сегодня существенно сократил время реконструкции, однако необходимо понимать, что это время является компромиссом между современными возможностями вычислительных алгоритмов (в том числе алгоритмов коррекции артефактов), производственной мощностью компьютеров, их ценой и решаемыми клиническими задачами. Иными словами, использование сложных математических алгоритмов способно уже сегодня на порядок повысить качество реконструкции ПДКТ-изображений, однако подобные вычисления пока еще требуют многих часов работы электронно-вычислительных машин (ЭВМ), что неприемлемо во время проведения интервенционно-радиологических вмешательств.
5. Порядок проведения ПДКТ-сканирования
На всех ангиографических комплексах плоский детектор закреплен на С-дуге и расположен напротив рентгеновской трубки, являющейся источником рентгеновского излучения (рис. 6). Такая конструкция, в отличие от гентри МСКТ, не ограничивает доступ к пациенту при проведении эндоваскулярных, чрескожных, внутрипросветных и комбинированных рентгенохирургических вмешательств как со стороны хирурга, так и со стороны анестезиологической бригады.
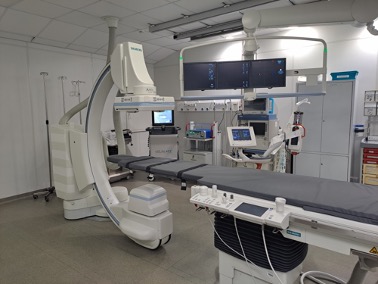
Рис. 6. Современный напольный ангиографический комплекс Artis Zee Floor (Siemens Healthineers, Германия), установленный в рентгеноперационной ОРХМДиЛ ФГБУ «НМИЦ онкологии им. Н.Н. Петрова» МЗ РФ. Ангиографический комплекс оснащен плоским детектором as40HDR размерами 40х30 см, что дает возможность выполнять двухфазную ПДКТ непосредственно во время рентгенохирургических вмешательств с применением как внутриартериального, так и внутривенного контрастирования. Программный пакет iGuide Needle Guidance (Siemens Healthineers, Германия) и лазерная подсветка позволяют использовать трехмерную чрескожную навигацию в режиме реального времени при проведении чрескожной биопсии, чрескожной энергетической абляции, чрескожного дренирования и других чрескожных вмешательств. Программный пакет Embolisation Guidance (Siemens Healthineers, Германия) позволяет использовать трехмерную внутрисосудистую навигацию в режиме реального времени при проведении суперселективной катетеризации и эмболизации/химиоэмболизации артерий, питающих опухоли печени и опухоли других локализаций, а также для автоматического поиска артерий, являющихся источником кровотечения. Программный пакет 3D/3D Fusion (Siemens Healthineers, Германия) позволяет выполнять слияние 3D-массивов данных, полученных посредством выполнения ПДКТ как с 3D-массивами других ПДКТ-исследований (выполненных на разных этапах вмешательства, например, до и после проведения микроволновой абляции), так и с 3D-массивами любых других модальностей лучевой визуализации, в том числе МРТ, МСКТ, ПЭТ-КТ и др.
ПДКТ-сканирование осуществляется путем поворота С-дуги вокруг тела пациента на 1800 + угол рентгеновского пучка (обычно составляющего 200) со скоростью рентгеновской съемки от 7,5 до 60 кадров в секунду, что позволяет получать до 500 2D-проекционных изображений, используемых для последующей реконструкции данных. Время сканирования (поворота С-дуги) может произвольно меняться от 3 до 20 с, что влияет на число полученных проекционных 2D-изображений и, соответственно, на контрастное и пространственное разрешение реконструируемых данных. От длительности сканирования и числа проекций также напрямую зависит лучевая нагрузка и выраженность артефактов движения, поэтому всегда следует искать компромисс между достаточным контрастным, оптимальным пространственным и минимальным временным разрешением, а также дозой излучения, получаемой пациентом.
Нужно помнить о том, что малейшее движение или дыхание пациента во время сканирования (поворота С-дуги) приводит к катастрофическому ухудшению качества реконструируемых изображений (рис. 4). В связи с этим пациентам, находящимся в сознании нужно объяснять важность соблюдения неподвижности и задержки дыхания в момент сбора данных. Пациентам, находящимся на ИВЛ, необходимо останавливать дыхание с исключением возможности его спонтанного возобновления.
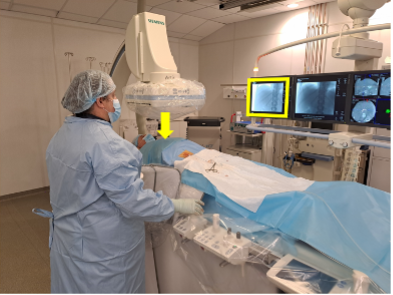
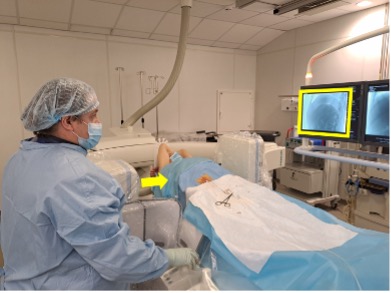
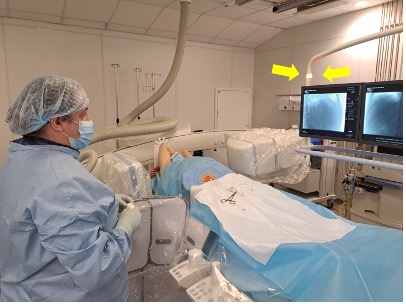
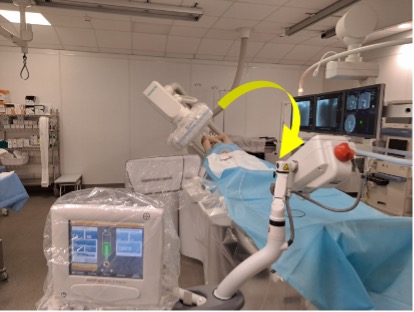
Рис. 7 (а-г). Этапы подготовки аппаратуры к проведению ПДКТ-сканирования (объяснения в тексте).
При проведении ПДКТ максимальное поле обзора (field of view, FOV) напрямую зависит от размеров плоского детектора, составляя 25x25x18 см для детекторов размерами 40х30 см и 25x25x25 см для детекторов размерами 41х41 см. Это необходимо иметь в виду и располагать пациента на операционном столе таким образом, чтобы зона интереса всегда находилась в центре FOV, то есть в центре вращения С-дуги. При этом сканирование головного мозга или предстательной железы не представляет трудностей, однако для исследования органов, смещенных вправо или влево (например, печени или селезенки), требуется определенный навык правильного размещения пациента на ангиографическом столе. Контроль позиционирования осуществляется путем тестового вращения С-дуги перед началом сканирования с визуализацией целевого органа в рентгеноскопическом режиме в прямой и боковой проекциях (рис. 7 А, Б). Тестовый прогон необходим также для исключения столкновения С-дуги с телом пациента, операционным столом и/или окружающей аппаратурой. Кратковременное включение рентгеноскопии перед запуском ПДКТ (рис. 7 В) необходимо для инициализации автоматического контроля экспозиции, который поддерживает фиксированное напряжение на лучевой трубке, модулируя только силу тока во время проведения сканирования (рис. 7 Г). Постоянное напряжение необходимо для предотвращения любых колебаний энергии луча, которые приводят к противоречивым данным оценки затухания и искажениям изображения [3, 37]. При сканировании органов брюшной полости руки пациента необходимо располагать за головой для снижения лучевой нагрузки, уменьшения уровня рассеянной радиации и улучшения контрастного разрешения получаемых изображений (рис. 8).
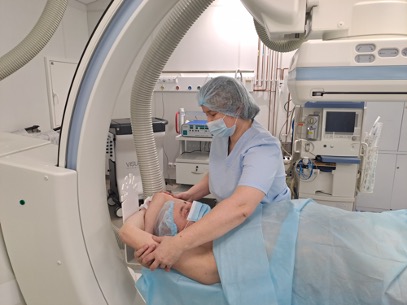
Рис. 8. Правильное и комфортное расположение пациента на ангиографическом столе, а также проведение инструктажа по задержке дыхания являются важными этапами подготовки к проведению интервенционно-радиологических вмешательств с использованием ПДКТ-технологий (объяснения в тексте).
6. Реконструкция изображений
Алгоритмы реконструкций ПДКТ-изображений исторически развивались по двум параллельным направлениям – аналитической реконструкции (filter-back-projection, FBP) и итеративной реконструкции (iterative reconstruction, IR). Однако следует отметить, что в последние годы к ним добавился и так называемый «гибридный метод с глубоким машинным обучением» [3, 4, 37, 40]. Основой реконструкции изображений, получаемых с помощью ПДКТ традиционно является математический алгоритм Фельдкампа-Дэвиса-Кресса (ФДК), реализованный в виде формулы свертки и обратного проецирования множества двухмерных проекций для прямой реконструкции трехмерной функции плотности, позволяющий получать трехмерные изображения большого объема и хорошего качества с использованием широкого рентгеновского луча пирамидальной формы за один поворот сканирующей системы, состоящей из одного источника излучения и одного плоского детектора [2]. Усовершенствованный метод обратной проекции с фильтрацией ПДКТ-изображений в настоящее время заключается в предварительной логарифмической обработке 2D-проекций с коррекцией недостатков детектора, повышением жёсткости пучка и компенсацией рассеяния, а также в использовании фильтра верхних частот и взвешивании коротких сканирований с последующей трёхмерной обратной проекцией на декартовой системе координат [3, 4, 37, 40]. Этот алгоритм лежит в основе подавляющего большинства ПДКТ-исследований, поскольку он быстр и надёжен для полностью дискретизированных круговых развёрток, получаемых при использовании круговых орбит сканирования.
В то же время для уменьшения недостатков рентгеновских пучков пирамидальной формы в последние годы были предложены так называемые некруговые траектории сканирования, в частности реализованная компанией Siemens Healthineers (Германия) технология сканирования по синусоидальной траектории (Sine Spin), улучшающая охват 3D-частот и уменьшающая артефакты, характерные для круговой орбиты вращения С-дуги. В данном случае для получения изображений необходим модифицированный алгоритм ФДК с использованием реконструкции с учетом выборки, при котором проектирование траектории и взвешивание оптимизируются совместно с проведением реконструкции [38, 39, 47].
Для повышения эффективности дозы и контроля артефактов в последние годы были внедрены также итерационные и регуляризованные методы математической обработки получаемых массивов данных. Регуляризация с использованием штрафного правдоподобия и TV-подобного метода подавляет шум и полосы в разреженных и низкоскоростных протоколах, обеспечивая лучшую основу для количественных задач, таких как паренхиматозное контрастирование и картирование перфузии (например, «виртуальной паренхиматозной перфузии») [48, 49]. Дополнительное шумоподавление на основе глубокого машинного обучения все чаще сочетается с итеративными конвейерами, улучшая соотношение сигнал/шум при более низкой дозе [50].
На первых ангиографических установках, оснащенных ПДКТ, реконструкция изображений занимала несколько минут, а в настоящее время осуществляется почти мгновенно. Реконструированные изображения в виде результирующего набора вокселей могут быть визуализированы либо в виде кроссекционных срезов, либо в виде 3D-изображений с применением любых просмотровых режимов используемых в клинической рентгенологии (MIP, MPR, MinIP, VRT, SSD, виртуальная эндоскопия, обзорная рентгенография, ротационная рентгенография, рентгеновская томография и т.д.), как непосредственно в рентгеноперационной, так и на отдельной рабочей станции ангиографической установки (рис. 9 А). Кроме того, с использованием программных пакетов для чрескожной и внутрисосудистой стереотаксической навигации, часть реконструированной информации может быть передана в стереотаксическое пространство ангиографической установки (рис. 9 Б. В). При этом она будет отображаться на рентгеноскопических мониторах рентгеноперационной в режиме реального времени, накладываясь на «живое» рентгеноскопическое изображение (режим дополненной рентгеноскопии), что является очень полезным при проведении многих чрескожных, эндоваскулярных и внутрипросветных рентгенохирургических вмешательств, что будет обсуждено ниже (рис. 9 Г).

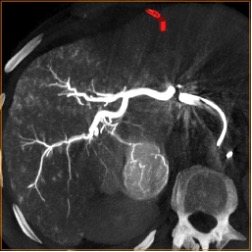
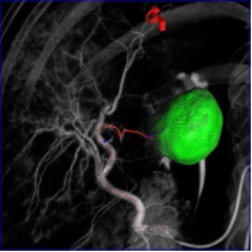
Рис. 9 (а-г). Этапы реконструкции и использования ПДКТ-изображений и ПДКТ-навигации в рентгеноперационной (объяснения в тексте).
7. Артефакты ПДКТ и их устранение
Артефактами в компьютерной томографии принято называть несуществующие в реальности, но видимые на реконструированных кроссекционных изображениях аномалии визуализации тканей, которые могут быть связаны либо с самой технологией сканирования (особенностями аппаратуры и геометрией рентгеновского пучка), либо со свойствами сканируемых материалов (например, металлов, не пропускающих рентгеновские лучи). В основе большинства артефактов лежит несовершенство данных, поступающих в алгоритм реконструкции таких как полихроматичность рентгеновского излучения, рассеяние, наличие дефектных пикселей в детекторе и движение пациента.
Поскольку алгоритм ФДК является лишь базовым (грубым) алгоритмом реконструкции, при его использовании в изображении возникает достаточно большое число разнообразных артефактов, обусловленных как аппроксимацией данных, так и физическими аспектами получения ПДКТ-изображений с использованием рентгеновского пучка пирамидальной формы. Большой угол расхождения лучей пирамидальной формы и сильное рассеяние подавляют низкочастотный сигнал и приводят к затенению/выемке и полосам, а повышение жёсткости пучка дополнительно искажает затухание, особенно вблизи «плотных» материалов, таких как кости основания черепа или металлические импланты [37, 40]. Как было сказано ранее, при использовании круговой орбиты ПДКТ-сканирования аксиальная детализация ухудшается в направлении от средней плоскости, что приводит к характерному размытию ПДКТ-изображений, которое также увеличивается с увеличением расстояния от изоцентра к периферии в связи с недостаточной угловой дискретизацией (рис. 3) [3, 4]. Артефакты, непосредственно связанные с конструкцией детекторов, включают временное запаздывание, появление ореолов, а также неоднородность усиления пикселей и дефектные элементы, проявляющиеся в виде персистирующих полос и колец при отсутствии коррекции (математического удаления) этих дефектных элементов из матрицы [4, 51]. Усечение анатомических структур за пределами поля зрения (в связи с ограниченным FOV) приводит к затенению ярких/темных границ и визуализации полос в реконструированном объеме [51]. Движения пациента во время сканирования, а также дыхание, сердцебиение и пульсация артерий (в особенности при вмешательствах на печени) приводят к появлению артефактов движения в виде размытости изображений и характерных полос (рис. 4, рис. 5) [40, 41].
На современных ангиографических установках коррекция артефактов реконструкции при проведении ПДКТ начинается ещё до получения обратных проекций. Калибровка детектора в виде создания карт усиления/смещения, компенсация задержки, обнаружение и «удаление» (математическое) дефектных пикселей, а также предварительная обработка логарифмических данных уменьшают неоднородность фиксированного шаблона и ореолы, которые в противном случае приводят к появлению колец и полос в реконструируемых объемах [4, 51]. Правильный выбор того или иного протокола сканирования также оптимизирует качество получаемых изображений путем установки режима фильтрации, ширины импульса и мА, настраиваемых для улучшения первичной плотности потока и оптимизации отношения сигнал/шум в пределах допустимой дозы для каждой отдельно взятой области сканирования (голова, грудь, живот, малый таз, конечности) [42, 45]. Повышение жесткости пучка компенсируется физическими или полиномиальными коррекциями, применяемыми к необработанным или логарифмическим данным, что уменьшает «выпячивание» и «полосы» вблизи объектов с высокой рентгеновской плотностью (например, металлических спиралей или металлических имплантов). Оценка и компенсация рассеяния дополнительно восстанавливают низкочастотный контраст, который «теряется» из-за больших полей сканирования и больших углов рентгеновского пучка по оси Z [37, 40]. Коррекция рассеяния и жёсткости пучка осуществляется путем предварительной логарифмической калибровки, а также использования полиномиальных алгоритмов и аподизированных фильтров которые существенно уменьшают затенение и полосы в реконструируемых ПДКТ-изображениях [37]. Коррекция усечения учитывает анатомические структуры, выходящие за пределы детектора, стабилизируя интенсивность пограничных участков и контролируя распространение линейных артефактов в объёме [37, 51].
Таким образом для устранения артефактов, характерных для ПДКТ, помимо регулярной калибровки систем и выбора оптимальных режимов импульсной рентгеновской съемки во время ротации, в настоящее время применяются многочисленные математические вычисления, которые постоянно совершенствуются, что способствует постепенному нивелированию недостатков ПДКТ-сканирования и улучшению качества ПДКТ-визуализации. В частности, совсем недавно в практическую работу были интегрированы новые технологии итеративной и регуляризованной реконструкции и шумоподавления на основе машинного обучения и ИИ, позволяющие дополнительно улучшать отношение сигнал/шум и подавлять линейные артефакты при более низкой дозе облучения [50]. Новые стратегии, учитывающие движение, в частности такие как «биннинг дыхательной фазы» и «коррекция на основе модели», способны значительно уменьшить артефакты движения (в особенности при выполнении ПДКТ печени), являющиеся серьезной проблемой при проведении многих интервенционно-радиологических вмешательств [46, 52].
На сегодняшний день в экспериментальных моделях разработаны очень сложные математические формулы, которые позволяют полностью нивелировать практически все артефакты реконструкции ПДКТ-изображений, характерные для рентгеновских лучей конической и пирамидальной формы, но их практическая реализация в настоящее время ограничивается только одним – недостаточной вычислительной мощностью современных ЭВМ [46].
В то же время необходимо отметить, что только использование некруговых орбит сканирования с учетом выборки за пределами стандартного круга (например, синусоидальное вращение и новые оптимизированные задачеориентированные траектории ротации систем источник-детектор) может обеспечить равномерное трехмерное частотное покрытие, что способно не математически нивелировать, а реально существенно уменьшить число артефактов, характерных для ПДКТ, интегрированной в ангиографические комплексы [38, 39, 47].
8. Некруговые орбиты сканирования
В настоящее время основной «рабочей лошадкой» ПДКТ-визуализации в интервенционной радиологии, как уже было отмечено, является изоцентрическая круговая орбита «короткого сканирования», заключающаяся в выполнении одного оборота С-дуги на 180° плюс угол пучка рентгеновского излучения (чаще всего 200), позволяющая получать предсказуемый набор данных, необходимых для ПДКТ-визуализации на основе быстрой аналитической реконструкции с использованием ФДК-алгоритма. Этот способ сканирования является наиболее простым с учетом объективных механических ограничений возможностей вращения С-дуги. Тем не менее круговая орбита, хотя и позволяет получать объем данных, соответствующих условию достаточности Tuy, в настоящее время не полностью удовлетворяет современные потребности интервенционной радиологии [38, 39, 47].Связано это прежде всего с недостатком получаемых данных вне пределов изоцентра сканирования, что приводит к сложностям визуализации при решении многих клинических задач и проявляется, например, в отсутствии качественной визуализации структур задней черепной ямки в связи с наличием артефактов усиления луча от костей основания черепа [39].
Кинематика современных напольных и потолочных ангиографических установок позволяет смещать ось источник-детектор из плоскости вращения и тем самым «добирать» недостающие проекции по оси Z. Используя эти возможности недавно были разработаны и внедрены в клиническую практику так называемые некруговые или двухосные траектории сканирования, созданные для улучшения охвата 3D-частот и уменьшения артефактов пирамидального пучка излучения. В частности, предложенный компанией Siemens Healthineers (Германия) режим сканирования «Sine-Spin» предполагает при проведении ротации дополнительный кранио-каудальный наклон гентри, который изменяется синусоидально во время вращения, обогащая выборку по оси Z (Z-семплирование) и уменьшая размытость изображений вне средней плоскости изображения, не отказываясь при этом от рабочего процесса с одной разверткой [39]. Таким образом «двойная обвязка траектории» удовлетворяет усиленному условию Tuy даже при сканировании структур, располагающихся в основании черепа, что позволяет устранить артефакты полос на ПДКТ-изображениях. Проведенные исследования показали значительное улучшение визуализации структур задней черепной ямки (в первую очередь областей кровоизлияний после инсульта) во время проведения интервенционных нейрорадиологических вмешательств на этой области с использованием двухосевых траекторий сканирования [39, 53]. Таким образом на первом этапе двухосевые орбиты, реализованные в практике, доказали, что «лёгкая неплоскость» вращения C-дуги способна почти полностью устранить ключевые ограничения «короткого кругового сканирования», а именно неполный охват области исследования и связанные с этим артефакты полос и артефакты уплотнения луча (в первую очередь «металлические артефакты» и артефакты от костей основания черепа). Особенно перспективным является использование некруговых траекторий сканирования, на базе роботизированных ангиографических установок нового поколения, обладающих практически неограниченной степенью свободы движений.
9. Роботизированные ангиографические установки
Разработка в 2007 г. принципиально новой напольной ангиографической установки Artis zeego (Siemens Healthineers, Германия) на базе семиосевого промышленного робота KUKA LWR III (KUKA Systems, Германия) ознаменовала переход от классической ангиографической установки к полностью роботизированной платформе для проведения сложных диагностических и лечебных рентгенохирургических вмешательств. Заложенная кинематика дала оператору шесть степеней свободы движений вокруг пациента, позволяя смещать «локоть» без изменения положения рентгеновского пучка. Переход в 2016 г. к платформе ARTIS pheno (Siemens Healthineers, Германия) на базе робота KR QUANTEC (KUKA Systems, Германия) сохранил напольное исполнение, но кардинально обновил механику (рис. 10). В частности, легкомагниевый U-образный штатив позволил расширить краниокаудальный наклон до ±25°, а максимальная скорость вращения С-дуги достигла 45 °/с, что позволило получать 397 проекций всего за 5 с в стандартном протоколе DynaCT Body (Siemens Healthineers, Германия). Данная ангиографическая система стала основой для разработки и внедрения принципиально новых некруговых орбит ПДКТ-сканирования в интервенционной радиологии [54].
Сегодня роботизированные ангиографические установки сочетают в себе С-дугу с программируемым изоцентрическим движением, что обеспечивает воспроизводимые траектории ПДКТ и точное позиционирование мишени в изоцентре. Ранние описания роботизированных ангиографических ПДКТ-систем продемонстрировали возможности расширения диапазона позиционирования и точные, повторяемые траектории вращения, подходящие для получения ПДКТ-изображений, практически недоступных для напольных и потолочных ангиографических установок [4, 54]. Некруговые траектории роботизированного сканирования существенно обогащают Z-семплирование и уменьшают артефакты «коротких круговых орбит» и пирамидального пучка, базируясь в то же время на «классическом» для ПДКТ рабочем процессе с одной развёрткой [38, 39]. В настоящее время практической реализацией «роботизированной ПДКТ» с использованием ангиографической установки ARTIS pheno (Siemens Healthineers, Германия) в клинической практике является возможность выполнения двух новых видов некругового сканирования, а точнее сканирования с «разорванной траекторией»: 1. однофазное сканирование с поворотом гентри на 365⁰ и одновременным смещением С-дуги вдоль оси Z (режим DynaCT 360), позволяющее получить широкий FOV размерами 32х32х24 см; 2. двухфазное сканирование с поворотом гентри на 220⁰ в каждой из фаз сканирования и смещением гентри вдоль оси Z между двумя ротационными съемками (режим DynaCT Large Volume) с дальнейшей «склейкой» изображений, позволяющее получать массивы данных большого объема вытянутой формы с FOV размерами 43х43х18 см. Обе орбиты продемонстрировали также выраженное уменьшение артефактов от металлоконструкций по сравнению с классическим круговым сканированием, позволяя существенно улучшить визуализацию кортикальных костных структур и мягких тканей вокруг установленных металлических имплантов [55, 56].
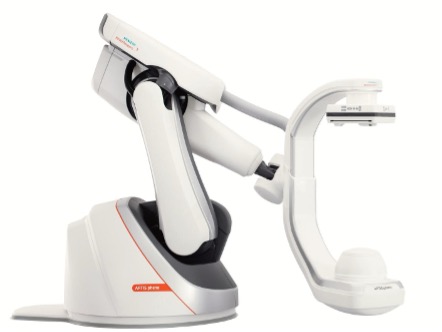
Рис. 10. Роботизированная напольная ангиографическая установка ARTIS pheno (Siemens Healthineers, Германия). Принципиальными отличиями данной системы от установки Artis Zee являются: 1. роботизированная (на базе робота KR QUANTEC, компании KUKA Systems, Германия) С-дуга с шестью осями вращения для точного позиционирования; 2. очень быстрый поворот C-Дуги во время сканирования (900/сек), что дает возможность выполнять ПДКТ в течение 3 сек; 3. усовершенствованный плоский детектор с 16-битовой матрицей позволяет получать томограммы со значительно более высоким контрастным разрешением, что является крайне важным для мягкотканной визуализации; 4. увеличенное до 130 см расстояние между лучевой трубкой и плоским детектором, существенно облегчает доступ к пациенту; 5. возможность сканирования с полным вращением С-дуги на 3600 позволяет обследовать сразу всю брюшную полость пациента (массив данных в виде цилиндра диаметром 32,0 см и длиной 23,5 см); 6. возможность выполнения ПДКТ любой части тела при любом положении пациента; 7. наличие гибкого изоцентра; 8. бесшовные герметичные поверхности, облегчающие дезинфекцию; 9. возможность лечения пациентов с массой тела до 280 кг (фотография с официального интернет-сайта компании Siemens Healthineers (Германия) (https://www.siemens-healthineers.com/ru/angio/artis-interventional-angiography-systems/artis-pheno, 04.12.2025)).
На основе роботизированных установок в настоящее время разрабатываются также принципиально новые траектории ПДКТ-сканирования в виде орбит, ориентированных на задачу (или задачеориентированные орбиты) которые в недалеком будущем позволят дополнительно улучшить качество ПДКТ-визуализации во многих сложных клинических ситуациях [55, 56]. В рамках этих разработок орбита сканирования больше не является фиксированной окружностью, но программируемой траекторией, определяемой под клиническую задачу, ограничения помещения и расстановку оборудования. При этом каждая орбита сканирования планируется и реализуется с помощью роботизированной кинематики, в то время как классические принципы ПДКТ-реконструкции в виде предварительной обработки, фильтрации и взвешивания по-прежнему остаются вычислительной основой [4, 37, 55, 56].
10. Лучевая нагрузка на пациента и персонал
В ранних экспериментах было показано, что при проведении высококонтрастных исследований, таких как ПДКТ-ангиография сонных артерий или ПДКТ грудной клетки, эффективная (поглощенная) доза существенно ниже той, которая фиксируется при выполнении МСКТ той же зоны. В то же время выполнение низкоконтрастных исследований, таких как ПДКТ органов брюшной полости приводит к получению пациентом сопоставимой с МСКТ эффективной дозы облучения [43-45]. Поскольку интервенционная радиология (рентгенохирургия) по определению является направлением с высокими дозами облучения она в своей работе всегда руководствуется принципом минимальной достаточности облучения ALARA («As Low As Reasonably Achievable», или «Как можно ниже, насколько это разумно достижимо») [57, 58]. Исходя из этого, ПДКТ целесообразно использовать во всех случаях, когда ее применение (за счёт снижения времени рентгеноскопии, или исключения необходимости выполнения повторных серий ЦСА) позволяет снизить суммарную лучевую нагрузку на пациента и персонал. Кроме того, использование ПДКТ представляется обоснованным в тех случаях, где оно снижает риски развития серьезных осложнений, а также может изменить план лечения на более эффективный.
Радиационное воздействие при ПДКТ характеризуется с помощью произведения дозы на площадь (DAP) и референтной воздушной кермы в контрольной точке интервенции, а не CTDI [57]. Эти показатели более точно отражают лучевую нагрузку при использовании широкого рентгеновского пучка пирамидальной формы и изменчивую геометрию облучения, характерную для ангиографических установок. Доза облучения пациента зависит от многих параметров, в том числе потенциала трубки, длительности импульса и силы тока (мА) на проекцию, частоты кадров, количества проекций, добавленной фильтрации (например, при использовании медного фильтра), расстояния от источника до изображения и используемой коллимации, а также от длины и типа траектории вращения при проведении сканирования. Например, при вращении рентгеновской трубки во время ротационной рентгенографии за спиной пациента, нагрузка на хрусталики глаз во много раз ниже, чем при вращении той же трубки со стороны живота [37, 42, 57]. Сравнительные исследования показывают, что однократное ПДКТ-сканирование может быть сопоставимо по дозе с несколькими ЦСА-сериями общей продолжительностью примерно 20 с, или с одной минутой импульсной рентгеноскопии [43, 44, 45]. Нужно также помнить, что распределение доз зависит от поля зрения, фильтрации и настроек экспозиции, поэтому тщательная настройка или выбор параметров (длительность импульса, мАс, фильтрация) может существенно снизить дозу облучения без ущерба для качества ПДКТ-визуализации [43-45]. Как показали многочисленные исследования, при проведении сложных эндоваскулярных вмешательств (прежде всего на сосудах головного мозга и печени) обоснованное выполнение ПДКТ с контрастным усилением заменяет несколько серий ЦСА, потенциально снижая общую дозу облучения пациента и улучшая обнаружение целевых очагов и питающих их артерий [27, 59]. В недавних публикациях также было показано, что современные инструменты ПДКТ-планирования и виртуальной ПДКТ-ангиографии позволяют дополнительно сократить число реальных ангиографических исследований, также снижая суммарную дозу облучения [23, 60]. Согласно опубликованным данным, уже сегодня использование методов ИИ и глубинного машинного обучения позволяет сократить дозу облучения примерно на 30% без потери качества изображений [40, 50, 51].
Важно отметить, что контроль движений пациента (неподвижное комфортное положение, задержка дыхания и др.) во время сканирования предотвращает необходимость проведения повторных ПДКТ-сканирований, что также снижает общую лучевую нагрузку [41]. В современных обзорах особое внимание уделяется перспективным протоколам сканирования, ориентированным на цель (целеориентированные орбиты), а также возможностям итеративного ИИ-ассистированного шумоподавления с целью получения «достаточных» (для проведения лечебных вмешательств) по качеству изображений при существенно меньшей экспозиции дозы [50, 61].
11. Терминология
В литературе за 20 лет было предложено множество названий ПДКТ, используемой в области интервенционной радиологии, отражающих этапы развития технологии, конструкцию плоского детектора, геометрию рентгеновского пучка, а также области клинического применения. На ранних этапах развития в англоязычной литературе использовался термин «Flat-Panel Volume Computed Tomography» («Плоско-Панельная Объемная Компьютерная Томография») отражающий возможность получения трехмерных объемных изображений с помощью цифровой «плоской панели». Эта формулировка была распространена в основополагающих описаниях физических принципов и конструкционных особенностей первых плоскодетекторных систем [4]. В эндоваскулярной хирургии, на начальных этапах, использовался термин «3D Rotational Angiography», или «3D RА» («3D Ротационная Ангиография») отражающий исторический аспект формирования направления и способ проведения сканирования [43, 44]. В настоящее время словосочетание «ротационная рентгенография» с нашей точки зрения, допустимо использовать только для описания способа сканирования, что и было отражено в начале работы при определении понятия ПДКТ. В то же время новые некруговые орбиты сканирования с разорванной траекторией, в том числе ПДКТ-сканирование, выполняемое по технологии томосинтеза, уже не может быть описано этим термином, что необходимо учитывать в будущем при внедрении этих технологий в клиническую практику [47, 55, 56].
Производители ангиографических установок при выпуске коммерчески-доступных систем с возможностью выполнения ПДКТ в 2004-2005 гг. также добавили путаницы называя одну и ту же технологию ПДКТ-сканирования различными коммерческими названиями, такими как «DynaCT» у компании Siemens Healthineers (Германия), «XperCT» у Philips (Голландия), «Innova3D» и «InnovaCT» у GE (США). Поэтому единого названия данной технологии, применяемой в области интервенционной радиологии, в мировой литературе до сих пор не существует.
Очень распространенным в англоязычной литературе является словосочетание «Cone Beam Computed Tomography», «Cone Beam CT» или «CBCT» («Конусно-Лучевая Компьютерная Томография» или «КЛКТ») характеризующее геометрию рентгеновского пучка. Однако, конический пучок рентгеновского излучения более характерен для предыдущего (первого) поколения сканирующих систем на базе С-дуг с электронно-оптическим преобразователем (ЭОП) вместо плоских детекторов, что подробно было обсуждено нами ранее в предыдущей работе (рис. 11) [2]. Учитывая тот факт, что в плоскодетекторных системах геометрия рентгеновского пучка более соответствует пирамидальной форме (рис. 12), словосочетание «конусно-лучевая компьютерная томография» нельзя считать оптимальным для описания ПДКТ и ее производных.
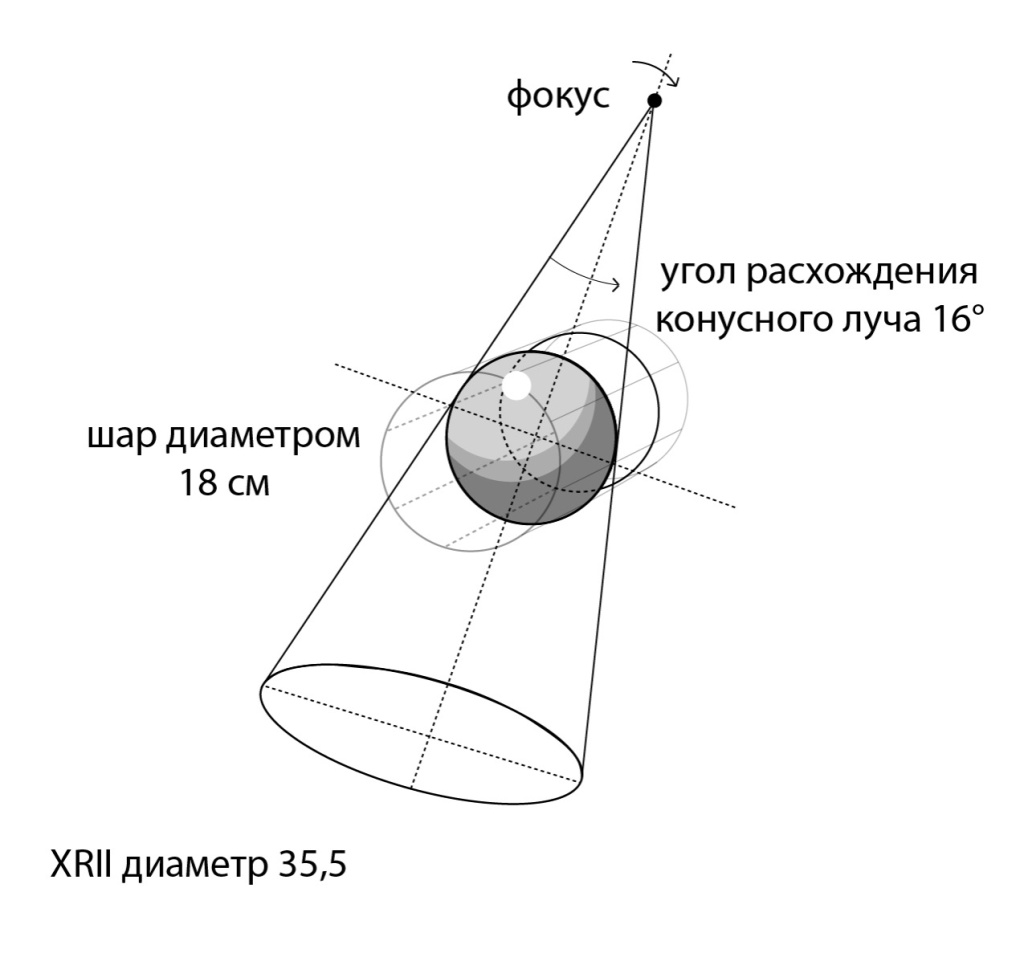
Рис. 11. Схематичное изображение конического луча с большим углом расхождения, применяемого при проведении конусно-лучевой компьютерной томографии с использованием электронно-оптического преобразователя (ЭОП, или XRII) диаметром 24 дюйма (35,5 см) [2].
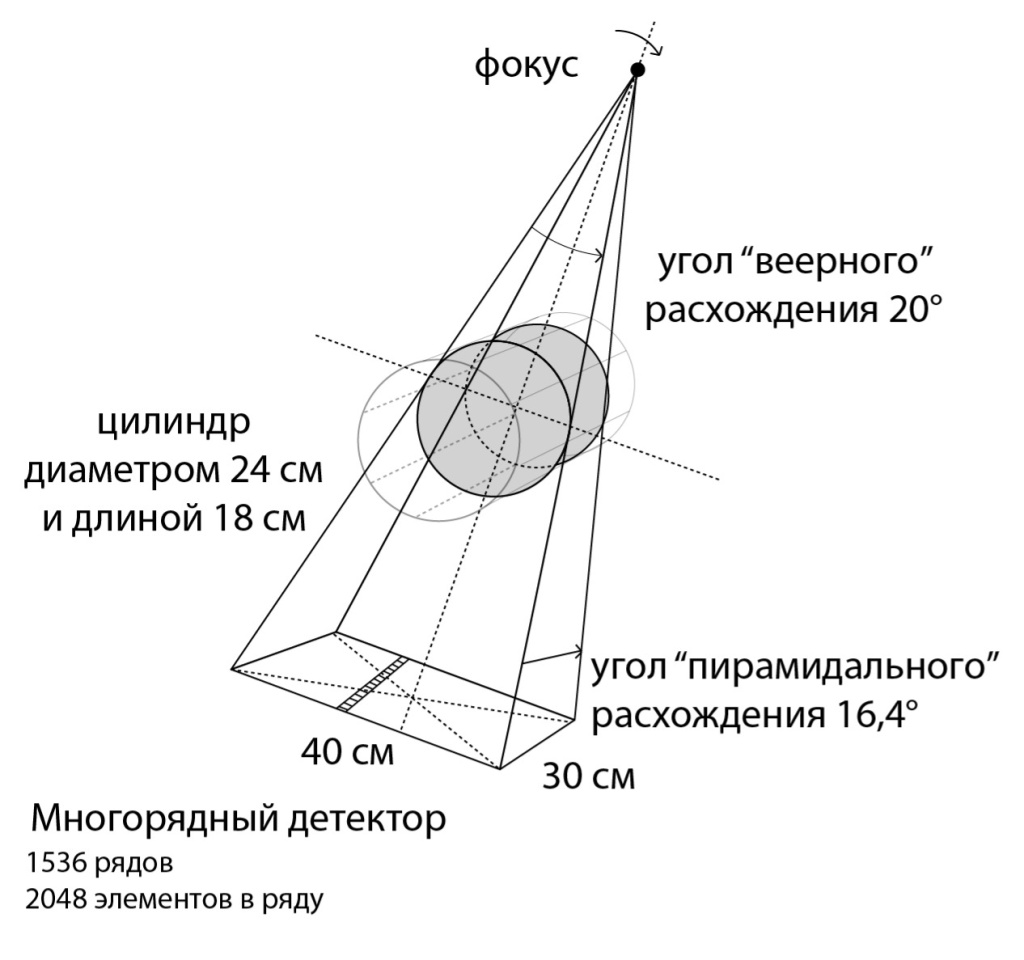
Рис. 12. Схематичное изображение пирамидального луча, применяемого при проведении ПДКТ с использованием плоского детектора размерами 30х40 см со 1536 рядами пиксельных элементов [2].
Также популярным в англоязычной литературе является словосочетание «C-arm Cone-Beam CT», «C-arm CT», или «CACT» («Компьютерная Томография на С-дуге», «КТ на С-дуге»), использовавшееся в ранних работах по чрескожной навигации и чрескожной энергетической абляции для обозначения «объемной компьютерной томографии», получаемой с использованием С-дуги, а не гентри МСКТ-сканера [13, 62]. Однако, учитывая бурное развитие роботизированных систем и имея в виду, что уже сегодня в клинической практике доступны диагностические рентгеновские аппараты, способные выполнять ПДКТ-сканирование с использованием двух независимых роботизированных гентри потолочного типа к одной из которых крепится рентгеновская трубка, а к другой плоский детектор (например, роботизированный рентгеновский комплекс Multitom Rax (Siemens Healthineers, Германия), можно предположить, что конструкция ангиографических установок в будущем также может уйти от использования С-дуги как единственного варианта гентри. В связи с этим, по нашему мнению, технологию ПДКТ, используемую в интервенционной радиологии не следует ограничивать конструкцией C-дуги. Кроме того, термин «C-arm CT» впервые был использован для описания сканирующих систем на основе ЭОП (еще до изобретения плоских детекторов) в связи с чем он не вполне точно отражает рассматриваемую в данной работе технологию.
С нашей точки зрения наиболее правильным названием технологии является «Flat-Detector Computed Tomography» («FDCT») или «Плоскодетекторная Компьютерная Томография» («ПДКТ»), впервые предложенное создателем спиральной компьютерной томографии и одним из основоположников ПДКТ немецким инженером W.A. Kalender в 2007 г. [3, 36]. В настоящее время этот термин используется во многих зарубежных технических и клинических руководствах, в особенности в области интервенционной нейрорадиологии, а также получил широкое распространение в русскоязычной медицинской литературе. При этом использование словосочетания «ПДКТ на С-дуге» («С-arm FDCT») может быть целесообразно только при первом упоминании технологии, указывая ее принадлежность к ангиографической установке, но в дальнейшем достаточно аббревиатуры «ПДКТ» («FDCT»), так как других вариантов компьютерной томографии, интегрированной в гентри С-дуги в настоящее время не существует. Важно, что для описания плоских детекторов нового поколения, например, двухэнергетических детекторов или детекторов прямого преобразования, предназначенных для компьютерной томографии с подсчетом фотонов в будущем можно будет также использовать термин ПДКТ, уточняя конструкцию детектора (например, двухэнергетическая ПДКТ, ПДКТ с подсчетом фотонов или ПДКТ прямого преобразования и т.д.) [63].
Эффективные ПДКТ-технологии, доступные для клинического использования
1. Технологии слияния изображений (fusion)
Создание ПДКТ превратило рентгеноперационную в полноформатный гибрид визуализационных технологий благодаря которому реконструированные объемы проведенных ранее исследований (МСКТ, МРТ, ПЭТ-КТ и др.) вместе с ПДКТ-исследованиями, выполненными во время рентгенохирургических вмешательств с помощью технологий слияния изображений (fusion) можно «принести прямо на операционный стол» наложив на «живую рентгеноскопию». Это позволило полностью отказаться от так называемой «ментальной тригонометрии» и «когнитивного фьюжена», сократить расход контрастных препаратов и время рентгеноскопии, а также начать эффективно выполнять многие вмешательства, проведение которых ранее было практически невозможно с использованием только плоскостных изображений (рис. 13). Процесс слияния (fusion) требует выполнения нескольких последовательных этапов: импорта и сегментации изображений, регистрации их с данными «текущего» (актуального) ПДКТ-исследования с использованием «ригидных» или «эластичных» 3D-3D протоколов объединения изображений, а также передачи (при необходимости) «результирующей виртуальной маски» в стереотаксическое пространство, где она начинает «жить» в общей с рентгеноскопическим изображением системе координат.
Рис. 13 (а-г). Этапы различных рентгенохирургических вмешательств, проведение которых ранее было невозможно на ангиографических установках, не оснащенных ПДКТ и опциями ПДКТ-навигации
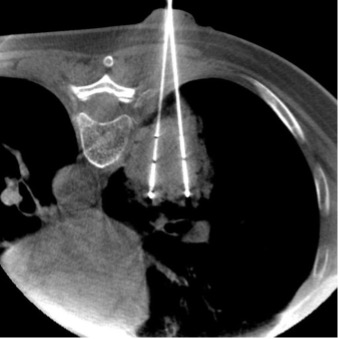
Рис. 13а. Криоабляция метастаза колоректального рака в лёгком (этап визуализации ледяного шара после первого цикла замораживания опухоли с использованием двух криозондов)

Рис. 13б. Криоабляция опухоли малого таза (этап визуализации ледяного шара после второго цикла замораживания опухоли с использованием трех криозондов)
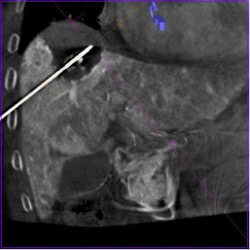
Рис. 13в. Микроволновая абляция узла гепатоцеллюлярного рака стадии BCLC A сразу после выполнения его суперселективной трансартериальной химиоэмболизации (этап визуализации зоны абляции, содержащей «призрак опухоли» сразу после окончания подачи энергии)
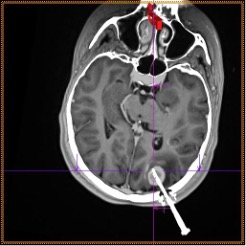
Рис. 13г. Стереотаксическая биопсия опухоли головного мозга под ПДКТ-контролем (этап контроля положения биопсийной иглы в опухоли с использованием объединенных (совмещенных) данных: ПДКТ для визуализации иглы и МРТ для визуализации опухоли)
Технологии слияния изображений, использующиеся сегодня в интервенционной радиологии целесообразно разделять на три большие группы. Первая подразумевает слияние определенного массива данных, полученного с использованием ПДКТ с массивом данных от «диагностических модальностей», для которых предполагается большая диагностическая ценность в связи преимуществами того или иного метода исследования (например, слияние ПДКТ/ПЭТ-КТ для взятия биопсии из метаболически активной части опухоли легкого). Для этого осуществляют объединение ПДКТ-массива данных с массивом данных диагностической МСКТ, МРТ или ПЭТ-КТ формате DICOM, а совмещенную информацию (например, о размерах и положении метастаза в печени) накладывают на рентгеноскопию в режиме реального времени с целью проведения таргетирования опухоли во время абляции или взятия биопсии [13, 64]. Основным недостатком такого слияния является то, что информация от разных модальностей, как правило, получается в разные фазы задержки дыхания или положения тела пациента, что делает проведение точного слияния технически очень сложным либо вообще неосуществимым. В будущем эти проблемы возможно будут решены с использованием ИИ-программ, которые в настоящее время еще не дошли до стадии коммерческой реализации. Вторым недостатком слияния «разных модальностей» является «устаревание» информации, полученной на диагностическом этапе. Так, даже при слиянии данных МРТ или МСКТ с данными ПДКТ, несущими информацию о размере и положении опухолей головного мозга (положение и размеры интракраниальных образований не зависят от дыхания и движения тела пациента) перед проведением стереотаксической биопсии, данные, полученные на диагностическом этапе, часто расходятся с данными интрапроцедурной ПДКТ-визуализации, так как глиобластомы могут значительно увеличиваться, а лимфомы наоборот уменьшаться в объеме (на фоне проведения гормонотерапии) за короткий промежуток времени [65]. Таким образом, использование мультимодального слияния изображений (ПДКТ/МСКТ, ПДКТ/МРТ и др.) в настоящее время может быть эффективным при осуществлении вмешательств только на малоподвижных органах (например, на позвоночнике) и только при медленно прогрессирующих заболеваниях (например, во время установки стент-графта в аорту для лечения аневризмы). Поэтому расширение возможностей интраоперационной ПДКТ-визуализации с использованием наиболее эффективных режимов контрастирования является краеугольным камнем повышения дальнейшей точности и безопасности проведения многих рентгенохирургических вмешательств, в том числе ПДКТ-контролируемой стереотаксической биопсии опухолей головного мозга [65].
Более надежным является использование интраоперационного слияния ПДКТ/ПДКТ массивов данных во время ряда интервенционно-радиологических процедур. В качестве примера можно привести возможность слияния данных ПДКТ-артериогепатикографии, несущей информацию о положении и размерах метастаза в печени с данными ПДКТ-артериогепатикографии после выполнения чрескожной энергетической абляции для получения информации о «крае абляции» (по аналогии с краем резекции) с целью оценки технической эффективности проведенного лечения [14, 24].
Третьим вариантом слияния изображений является наложение данных, полученных с помощью ПДКТ-сканирования (или изображений других модальностей) на «живую рентгеноскопию» при проведении чрескожной, внутрисосудистой и внутрипросветной навигации, что будет более подробно рассмотрено в следующем разделе.
2. Технологии дополненной реальности
Технологии дополненной реальности (дополненной рентгеноскопии) на основе ПДКТ подразумевают возможность проецирования трехмерной информации, полученной с помощью ПДКТ, непосредственно на рентгеноскопические мониторы в рентгеноперационной в режиме реального времени, что позволяет видеть анатомические структуры и «мишени» «на месте» во время использования рентгеноскопии. Типичный рабочий процесс включает получение ПДКТ-изображений, сегментацию сосудов, целевых очагов и других необходимых структур, вычисление трехмерной карты и регистрацию этой модели совместно с геометрией С-дуги, чтобы наложение синхронизировалось с движениями гентри и стола в стереотаксическом пространстве ангиографической установки. Эта парадигма, часто называемая также «3D-картированием в реальном времени» или «3D-роадмапингом», широко используется как практичный и быстрый способ преобразования данных ротационной рентгенографии в руководство к дальнейшему проведению рентгенохирургических вмешательств [66, 67]. В настоящее время технологии дополненной реальности широко используются для проведения чрескожной, эндоваскулярной и эндобронхиальной навигации.
2.1. Чрескожная навигация
Рис. 14 (а-г). Использование различных видов контрастирования при выполнении некоторых лечебных чрескожных рентгенохирургических вмешательств под контролем ПДКТ-навигации
Рис. 14а. Контроль положения иглы в остеолитическом метастазе тела позвонка перед проведением вертебропластики (ПДКТ без дополнительного контрастирования)
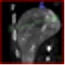
Рис. 14б. Построение траектории установки криозонда для проведения чрескожной аргоно-гелиевой криоабляции метастаза колоректального рака в печени (внутриартериальное контрастирование в виде капиллярной фазы ПДКТ-артериогепатикографии)
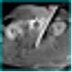
Рис. 14в. Контроль положения криозонда перед проведением чрескожного крионейролизиса чревного сплетения у пациента с болевым синдромом, обусловленным раком головки поджелудочной железы (ПДКТ на фоне внутривенного контрастирования)
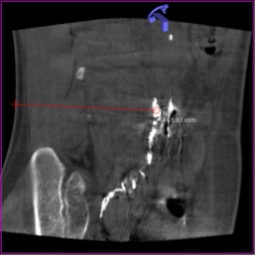
Рис. 14г. Построение траектории установки иглы в полость лимфопсевдоаневризмы забрюшинного пространства для выполнения чрескожной эмболизации места утечки лимфы с целью лечения массивной послеоперационной лимфореи (ПДКТ с использованием интранодальной паховой лимфангиографии)
Стандартный рабочий процесс начинается с выполнения ПДКТ без контраста (например, для биопсии или абляции опухолей легких) или с использованием внутриартериального (например, для абляции узлов ГЦР в печени), внутривенного (например, для проведения крионейролизиса), эндолимфатического или других видов контрастирования (рис. 14). Далее на рабочей станции выполняется полуавтоматическая или автоматическая сегментация (выделение) целевых и критически важных структур, а также интерактивное построение безопасной траектории чрескожного таргетирования путем установки двух точек, одна из которых располагается в целевой зоне, а вторая – в точке входа аппликатора на коже. Далее, в автоматическом режиме, осуществляется построение трассы таргетирования и после оценки ее безопасности (избегание крупных сосудисто-нервных пучков, полых органов и др.) она регистрируется в стереотаксическом пространстве («геометрии») С-дуги таким образом, что 3D-карта накладывается на рентгеноскопическое изображение и обновляется вместе с изменением положения гентри, что позволяет совмещать иглу или аппликатор с прогнозируемой целью в режиме реального времени [62, 66]. Дополнительные опции наведения иглы, такие как захват цели, подсвечивание ортогональных (взаимно-перпендикулярных) проекций с помощью лазера, информирование врача о глубине установки аппликатора, предназначены для уменьшения числа ошибок и очень помогают при таргетировании с использованием сложных углов атаки, а также в случаях «длинных траекторий», проходящих через подвижные органы (рис. 15). При проведении энергетической абляции, биопсии и других чрескожных вмешательств после установки иглы или аппликатора в целевую область обязательно проводится повторное ПДКТ-сканирование для подтверждения адекватного расположения устройства в целевой зоне. Ранее было показано, что использование технологий чрескожной стереотаксической навигации значительно облегчает проведение чрескожных вмешательств, в особенности при таргетировании образований диаметром менее 10 мм, не визуализируемых при УЗИ, повышая техническую эффективность и безопасность ряда процедур, в частности чрескожной биопсии опухолей легких [18, 64]. Более того, выполнение различных чрескожных рентгенохирургических вмешательств (биопсия, дренирование, абляция и т.д.) под ПДКТ-контролем осуществляется значительно быстрее, точнее и технически более эффективно по сравнению с выполнением тех же вмешательств под контролем МСКТ, при этом эффективная доза облучения на 13-42% меньше [68-71].
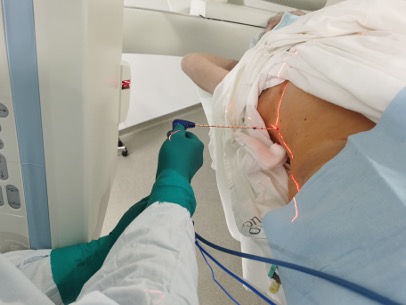
Рис. 15. Введение антенны для микроволновой абляции в опухоль печени под контролем ПДКТ с использованием штатной лазерной подсветки ангиографического комплекса Artis Zee (Siemens Healthineers, Германия): после выполнения ПДКТ-артериогепатикографии и определения безопасной траектории таргетирования С-дуга ангиографической установки устанавливается в положение «вид сверху», после чего автоматически включается лазерная подсветка, позволяющая без использования рентгеноскопии определить точку входа аппликатора на коже пациента; при правильном расположении аппликатора, согласно запланированной траектории таргетирования, визуализируется лазерная подсветка на всем протяжении шафта антенны для микроволновой абляции в двух взаимно-перпендикулярных проекциях, что позволяет без включения рентгеноскопии точно провести аппликатор в тело пациента на заранее определенную глубину.
2.2. Эндоваскулярная навигация
Технологии внутрисосудистой навигации на основе ПДКТ конфигурируют полученные во время ПДКТ-артериографии изображения артериального русла в интерактивную сосудоориентированную дорожную карту, которая также, как и в предыдущем случае совмещается, регистрируется и синхронизируется с текущей геометрией С-дуги. При этом возможно использование дополнительных специальных программных пакетов, предназначенных для полуавтоматического или автоматического поиска питающих опухоль артерий [72]. Как было показано ранее, данные программы позволяют значительно повысить выявляемость питающих опухоль артерий, сокращая общее время процедур ссТАХЭ, одновременно значимо улучшая как техническую эффективность выполняемых процедур, так и отдаленные результаты лечения [73]. После сегментации целевой опухоли и построения 3D-карты внутрисосудистой навигации (в виде «подсвеченной» внутрисосудистой траектории) информация передается в стереотаксическое пространство, что позволяет быстро и прецизионно провести проводник и микрокатетер вдоль трехмерных осевых линий под контролем дополненной рентгеноскопии непосредственно к точке планируемой ссТАХЭ без использования этапной ЦСА. В опубликованных работах новая парадигма использования «3D-дорожной карты в реальном времени» описывается как практичный и высокоэффективный способ преобразования отдельного 3D-изображения в полезное руководство для безопасной и прецизионной эмболизации/химиоэмболизации [30, 66, 67]. Более того, данная технология сокращает число дополнительных серий ЦСА, приводя к снижению лучевой нагрузки на пациента и персонал [27].
2.3. Эндобронхиальная навигация
Технология, в значительной степени похожая на вышеописанные, заключается в том, что после проведения бесконтрастного ПДКТ-сканирования органов грудной полости, дыхательные пути сегментируются и преобразуются в осевые линии и целевые модели. Эти модели (например, сегментированная периферическая опухоль легкого) затем накладываются на рентгеноскопическое изображение и постоянно обновляются с учетом движений гентри и стола, превращая единичную развертку в интерактивное руководство вместо статичного набора данных. Внутри дыхательных путей интралюминальная навигация может объединять ПДКТ с предоперационной МСКТ для согласования предпроцедурных дорожных карт с интрапроцедурной анатомией. Объединенная 3D-модель дыхательных путей регистрируется на С-дуге и используется для облегчения проведения бронхоскопа (или проводникового катетера) в режиме дополненной рентгеноскопии для выполнения трансбронхиальной биопсии, трансбронхиальной криоабляции или трансбронхиальной микроволновой абляции периферических злокачественных новообразований легких [74-76].
3. Технологии виртуальной реальности (ВР)
Если технологии дополненной реальности привнесли в операционную «трехмерные ПДКТ-изображения в режиме реального времени», то разработка программных пакетов на основе ВР способна превратить эти ПДКТ-изображения в «интерактивную 3D-сцену», внутри которой оператор может свободно «перемещаться», планировать варианты чрескожного и внутрисосудистого лечения, оценивать его «результаты» а также учиться, не подвергая ни себя, ни пациента дополнительному введению контрастных препаратов и дополнительной лучевой нагрузке. Иными словами, уже сегодня современные ВР-технологии позволяют использовать реконструированные ПДКТ-изображения как «виртуальный полигон» на котором можно точно смоделировать результаты и последствия проведения тех или иных чрескожных и эндоваскулярных рентгенохирургических вмешательств. В настоящее время широко используют три коммерчески доступные технологии виртуального планирования, однако в будущем к ним будут добавляться опции моделирования все большего и большего числа сложных интервенционно-радиологических процедур. В совокупности эти виртуальные инструменты на основе ПДКТ позволяют объединить этапы планирования, навигации и контроля эффективности ряда вмешательств в одной рентгеноперационной, делая ПДКТ предсказуемой и более «экономичной» с точки зрения использования контраста и облучения по сравнению с традиционными методами визуализации такими как рентгеноскопия и ЦСА [27, 60]. Опубликован ряд клинических исследований, свидетельствующих о том, что использование ВР-ангиографии и ВР-планирования чрескожной абляции или ссТАХЭ повышает техническую успешность процедуры, сокращая время операции и снижая лучевую нагрузку [60, 77]. Предполагается, что по мере совершенствования графических процессоров, 5G-стриминга и «голосовых ИИ-ассистентов» ВР-технологии на базе ПДКТ в рентгеноперационной могут стать столь же рутинным инструментом интервенционной радиологии, как в настоящее время сама ПДКТ и технологии дополненной реальности на ее основе [78].
3.1. Виртуальная абляция
Виртуальная абляция подразумевает использование специального программного обеспечения, превращающего интрапроцедурную ПДКТ в среду планирования и прогнозирования результатов чрескожной энергетической деструкции опухолей [79-81. С использованием данных программ врач может смоделировать и «увидеть» зону абляции, а также край абляции, размещая один или несколько виртуальных аппликаторов в целевом очаге. При этом система автоматически прогнозирует зону абляции в зависимости от вида (криозонды, антенны для МВА, электроды для РЧА и др.), параметров (в зависимости от производителя и каталожного номера конкретных устройств) и числа аппликаторов. Прогнозируемый объём абляции зависит также от «геометрии» установки аппликаторов и выбранных параметров подачи энергии (мощность, время, синергетический эффект и др.). Результирующая «виртуальная зона обработки» отображается в 3D-режиме на рентгеноскопических экранах, позволяя оператору оценить область абляции перед подачей энергии и скорректировать положение и число аппликаторов или продолжительность воздействия для обеспечения технической эффективности процедуры. Критические структуры (полые органы, артерии и др.) могут быть дополнительно сегментированы и вместе с траекторией таргетирования после «одобрения плана» зарегистрированы для дальнейшего использования в процессе вмешательства [79]. После завершения процедуры контрольная ПДКТ с контрастированием «документирует» реальную зону абляции и позволяет напрямую сравнить её с прогнозом, предлагая дополнительные «перекрывающие» сеансы энергетического воздействия в случае выявления недостаточного края абляции [80, 81]. Предполагается, что в недалеком будущем полученная после абляции информация о результатах лечения может быть возвращена обратно в программу для ее дополнительного (машинного) обучения, корректирующего предустановленные настройки в соответствии с реальной клинической практикой [79-81].
3.2. Виртуальная химиоэмболизация
Ключевая функция программных пакетов «виртуальной инъекции (эмболизации)» заключается в том, что полученные с помощью ПДКТ-артериогепатикографии данные используются для прогнозирования распределения контрастного препарата (а также химиоэмболизата) в печени и сегментированном целевом опухолевом узле при расположении «виртуального катетера» в любой части артериального русла. Таким образом, вместо проведения реальной этапной ЦСА (в 2D-режиме) методом проб и ошибок оператор виртуально «тестирует» различные уровни артериального дерева и выбирает оптимальную точку химиоэмболизации, позволяющую полностью перекрыть артериальное кровоснабжение опухоли с минимальным повреждением здоровой паренхимы печени. Использование данного программного обеспечения позволяет снизить число дополнительных ЦСА-серий и этапных ПДКТ-сканирований, что существенно сокращает расход контрастного препарата и лучевую нагрузку на пациента и персонал при сохранении качества планирования и проведения процедур ссТАХЭ [30, 60, 67]. Количественные опции программных пакетов включают в себя также возможность оценки «виртуальной паренхиматозной перфузии», благодаря чему перфузионные изменения после химиоэмболизации могут быть смоделированы заранее, что дополнительно облегчает правильный выбор целевого сосуда и оценку состояния паренхимы печени после процедуры [48, 49].
3.3. Виртуальная установка стент-графта
Программа виртуального стентирования («виртуальный стент-графт») включает в себя этапы планирования и наведения при которых виртуальная модель стент-графта помещается в трёхмерную анатомическую структуру, полученную с помощью ПДКТ, и в последующем проецируется на рентгеноскопическое изображение в режиме реального времени. После ротационного сканирования с внутриартериальным контрастированием аорта и магистральные артерии сегментируются, а также создаются осевые линии и контуры артериального русла. Далее макет предполагаемого стента или стент-графта подгоняется по размерам, полученным с помощью ПДКТ, и выравнивается по осевой линии. В дальнейшем зарегистрированная модель визуализируется в виде трёхмерной карты, которая отслеживает движение гентри и стола во время «живой рентгеноскопии» [82]. Рабочий процесс ориентирован на индивидуальный подбор размеров графта и точность его «посадки» для каждого конкретного пациента, находящегося в рентгеноперационной. Параметры диаметра и длины аневризмы, измеренные на ПДКТ-изображении в рентгеноперационной, определяют точный подбор имплантируемых устройств, а совмещенное наложение позволяет оператору проверить устья, точки разветвления и запланированные зоны установки в той проекции, которая будет использоваться для реальной имплантации. Поскольку «дорожная карта» совмещена с геометрией С-дуги (то есть погружена в стереотаксическое пространство ангиографической установки), проверенные виртуально координаты остаются неизменными при вращении С-дуги или смещении стола, что позволяет позиционировать проводники и катетеры, а также имплантировать стент-графт без выполнения дополнительных ПДКТ-сканирований [67, 82].
Перспективы дальнейшего развития ПДКТ и ПДКТ-технологий
Внедрение ПДКТ и ряда ПДКТ-технологий, описанных выше, уже сегодня изменило тактику проведения многих чрескожных и эндоваскулярных вмешательств [14, 24, 65]. Дальнейшее развитие этих технологий ближайшие 5-10 лет обещает нам переход на «новую квантовую ступень» благодаря ожидаемым прорывам в конструкции детекторов, разработке роботизированных орбит сканирования и совершенствовании ИИ-алгоритмов. Дальнейшее развитие ПДКТ-технологий будет связано также с улучшением ПДКТ-визуализации с параллельным снижением лучевой нагрузки на пациента и персонал, разработкой систем синхронизации дыхания и движений пациента во время проведения вмешательств, а также с развитием роботизированных систем для выполнения чрескожных и эндоваскулярных лечебных процедур. По всей видимости ангиографический комплекс с возможностью выполнения ПДКТ станет «технологическим ядром» в которое, по мере развития технологий, будут интегрироваться (сопрягаться) все новые дополнительные системы наведения, оптического и электромагнитного слежения (например, для отслеживания дыхания), лучевой визуализации (например, ультразвуковые сканеры), а также (по всей видимости) голографический интерфейс, позволяющий «видеть» анатомические структуры и инструменты не только на рентгеновских мониторах, но и через очки дополненной реальности [29, 78].
1. Новые конструкции плоских детекторов
Инновации в области детекторных технологий для ПДКТ на С-дуге в настоящее время развиваются по трем взаимодополняющим направлениям: 1. создание более быстрых и «малошумных» детекторов на основе CMOS-технологии; 2. разработка различных вариантов двухэнергетической ПДКТ; 3. конструирование детекторов с прямым преобразованием рентгеновского излучения в электрический сигнал с возможностью подсчета фотонов. Каждое из этих решений направлено на достижение одного и того же клинического эффекта – более высокого пространственного, временного и, в особенности, контрастного разрешения при как можно меньших дозах облучения [1].
Детекторы на основе технологии CMOS (комплементарного металло-оксидного полупроводника (complementary metal-oxide semiconductor)) сохраняют принцип непрямого преобразования на основе CsI, однако в них подлежащий слой a-Si заменен на так называемую CMOS-подложку состоящую не из аморфного, а из кристаллического кремния. Не вдаваясь в подробности необходимо отметить, что преимуществами такой конструкции является более мелкий размер пикселей (около 100 мкм), меньший электронный шум, уменьшенная задержка передачи изображений и гибкий режим работы с полным набором ячеек (без биннинга), что в совокупности обеспечивает протоколы с более высоким контрастным и пространственным разрешением и более стабильную визуализацию при более низких дозах облучения. В настоящее время коммерческое использование этих систем в интервенционной радиологии сдерживается так называемым «радиационным старением пикселей», ограниченным напряжением (< 130 кВ), а также сложностью и высокой ценой производства CMOS-панелей [1]. В то же время предварительные стендовые испытания ПДКТ на основе CMOS-технологии подтверждают важные преимущества данных детекторов, что позволяет надеяться на их внедрение в интервенционную радиологию в недалеком будущем [83].
Другим перспективным направлением считается двухэнергетическое сканирование, в первую очередь с использованием новых плоских детекторов, содержащих два сцинтилляционных слоя a-Si:H/CsI:Tl, разделенных тонким слоем меди и соединённых с отдельными электронными считывателями [84, 85]. Такая конструкция детекторов позволяет раздельно регистрировать низко- и высокоэнергетические сигналы в каждой проекции, обеспечивая надежное слияние бинарных данных и защиту их от артефактов движения. Это позволяет получать карты распределения йода с разделением материалов и объемы с высокой степенью жесткости пучка непосредственно в рентгеноперационной. Экспериментальные образцы двухэнергетических детекторов недавно продемонстрировали возможность и перспективность их использования в области интервенционной радиологии [84, 85]. С клинической точки зрения, ближайшие перспективы использования двухэнергетических панелей включают в себя возможность получения попроекционных йодных карт для планирования и контроля эффективности ссТАХЭ, а также двухэнергетических «дорожных карт», исключающих линейные артефакты вокруг плотных структур (например, установленных ранее в артерии головного мозга металлических спиралей и др.) и «дозонейтральных протоколов», заменяющих несколько ангиографических процедур одним «спектральным вращением». В долгосрочной перспективе двухэнергетическое ПДКТ-сканирование будет сочетаться с оптимизированными для конкретных задач траекториями и автоматизированным планированием, чтобы спектральная информация напрямую использовалась для проведения рентгенохирургических вмешательств с возможностью оценки перфузии [84, 85].
Другим вариантом получения двухэнергетических изображений является быстрое переключение кВ на рентгеновской трубке во время проведения ротационной съемки с использованием «классических» плоских детекторов первого поколения. Этот вариант является привлекательным в связи с относительной простотой его реализации, а также высокой устойчивостью получаемых изображений к движению пациента во время сканирования [86]. Быстрое переключение кВ обеспечивает независимый от детектора способ спектрального разделения за счет изменения потенциала трубки в течение одного оборота. Поскольку два спектра чередуются, а не получаются в ходе отдельных сканирований, минимизируется риск «несовмещения» изображений. Практическое применение технологии зависит от точной спектральной калибровки и коррекции рассеяния, зависящего от поля зрения и жёсткости пучка [86].
Третьим перспективным направлением улучшения качества визуализации ПДКТ-систем в будущем считается создание принципиально новых плоских детекторов где в качестве сцинтилляторов будут использоваться (например) кристаллы теллурида кадмия (CdTe), обладающие свойствами прямого преобразования рентгеновских лучей в электрический сигнал с дискриминацией их по энергии [63]. Первые лабораторные исследования таких детекторов продемонстрировали возможность пошагового или сегментированного получения изображений, меньшую временную задержку по сравнению с классическими детекторами непрямого преобразования и улучшенное отображение низкоконтрастных деталей благодаря спектральному биннингу. Все эти очевидные преимущества могут открыть путь к получению высококачественных настраиваемых и дозоэффективных ПДКТ-изображений при внедрении их в практику [63]. ПДКТ с подсчётом фотонов в перспективе позволит получать «многобиновые» спектральные данные с малой задержкой и улучшенной детализацией при низком контрасте, что можно рассматривать как естественное продолжение технологий двухэнергетической ПДКТ в интервенционно-радиологической практике [1, 63].
2. Новые роботизированные орбиты сканирования, ориентированные на задачу
Как было показано ранее, «круговое короткое сканирование» остается базовым для аналитической реконструкции, но его выборка неоптимальна для деталей вне средней плоскости и чувствительна к артефактам широкого угла излучения [37, 38]. Обзоры, посвященные перспективам использования новых роботизированных целеориентированных орбит сканирования, рассматривают будущие орбиты сканирования как нечто проектируемое для конкретного поражения, задачи и размеров рентгеноперационной. В экспериментальных исследованиях это позволяет перераспределять угловую выборку в сторону максимально информативных ракурсов и избегать использование малоэффективных углов вращения, демонстрируя преимущества в производительности по сравнению со стандартным кругом в условиях реалистичных ограничений гентри [55, 56]. В более широком смысле, «фреймворки оптимизации траектории» строят орбиту как задачу управления с ограничениями – с учетом столкновений, скорости и пределов дозы таким образом, что путь источник-детектор может быть настроен в соответствии с задачей визуализации и механическими характеристиками роботизированного комплекса [47] (рис. 16). Роботизированные ангиографические устройства обеспечивают точные, повторяемые некруговые орбиты и изоцентрическое позиционирование, удерживая цель в центре при реализации необходимой траектории. В перспективе, ориентированные на цель орбиты, оптимизированное взвешивание и итеративная ИИ-реконструкция смогут обеспечивать последовательный путь к повышению чёткости и снижению артефактов в рамках одного сканирования, разработанного с учётом клинической задачи [47]. Перспективными орбитами, ориентированными на задачу которые планируется в будущем интегрировать в клиническую практику являются следующие: 1. орбиты увеличения FOV (рис. 17); 2. орбиты многофазных исследований (например, для изучения паренхиматозной перфузии); 3. орбиты избегания столкновений (например, с дыхательной аппаратурой); 4. орбиты снижения дозы облучения; 5. орбиты подавления металлических артефактов (например, для улучшения мягкотканной визуализации паренхимы головного мозга после эмболизации аневризм спиралями). Предполагается, что большая часть орбит, ориентированных на задачу будет «строится» с использованием ИИ непосредственно в рентгеноперационной либо перед проведением ПДКТ, либо непосредственно в процессе ПДКТ-сканирования [47].
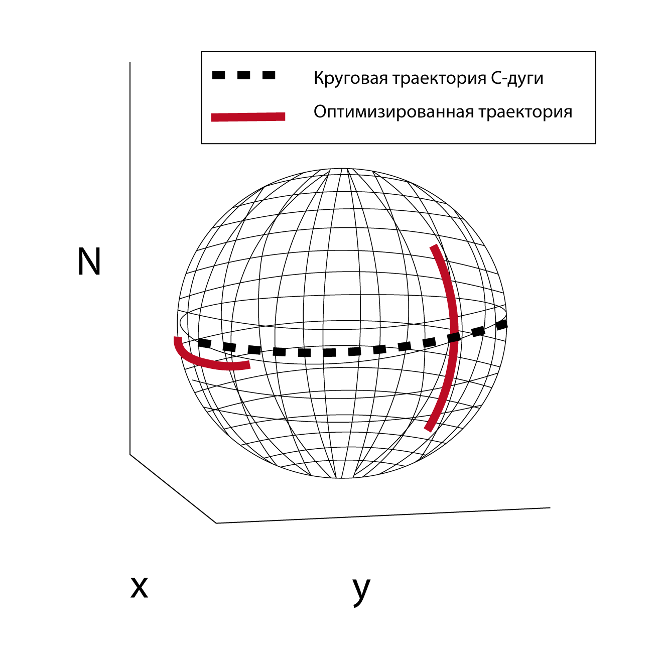
Рис. 16. 3D-визуализация траектории ПДКТ-сканирования, позволяющей избежать столкновения С-дуги с окружающим оборудованием (красная сплошная линия) в сравнении с «классической» короткой круговой траекторией (чёрная пунктирная линия) (адаптировано из [47]).
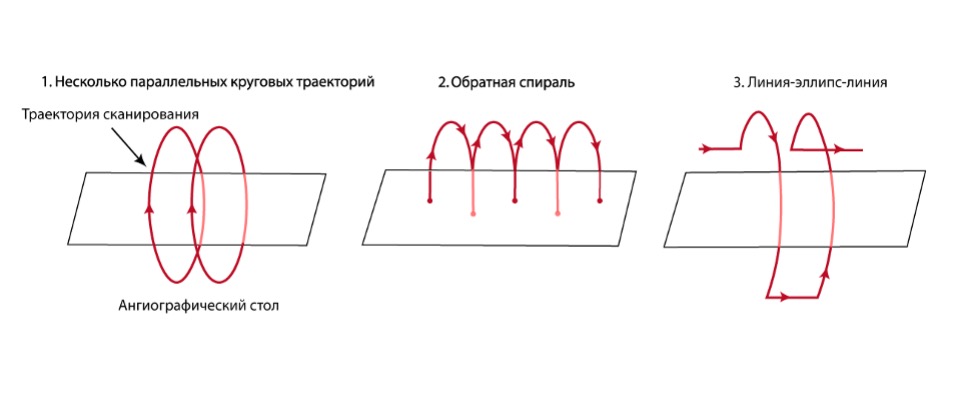
Рис. 17. Возможные варианты ПДКТ-сканирования с «задачеориентированной» орбитой, направленной на увеличение продольного поля зрения (FOV): 1. С использованием нескольких параллельных круговых траекторий; 2. С использованием траектории «обратная спираль»; 3. С использованием траектории «линия-эллипс-линия» (адаптировано из [47]).
3. Совершенствование программ ИИ и глубокого машинного обучения
Предполагается, что интеграция технологий ИИ и машинного обучения в процесс проведения ПДКТ будет развиваться по трем основным направлениям: 1. повышение уровня контроля текстуры шума при как можно более низкой дозе облучения; 2. разработка технологий реконструкции ПДКТ-изображений с учетом движений (пациента, органов, артерий и т.д.), нивелирующих артефакты движения при многосекундных ротациях; 3. совершенствование алгоритмов автоматической регистрации и сегментации слияния изображений (в особенности мультимодальных) с последующим использованием их для стереотаксического наведения и контроля.
Как было показано выше, ИИ и глубокое машинное обучение уже сегодня используются как эффективные вспомогательные инструменты, дополняющие реконструкцию изображений шумоподавлением, автоматизирующие извлечение анатомических структур и стабилизирующие наложение изображений во время навигации [30, 87, 88] . На практике шумоподавление на основе обучения улучшает соотношение контрастности и шума без увеличения экспозиции, помогая ПДКТ-изображениям соответствовать заданным требованиям к качеству. В будущем такие методы будут дополнительно совершенствоваться для более эффективной работы совместно с технологиями регуляризованной реконструкции и спектральной коррекции в едином ангиографическом программном пакете [50].
Движение пациента во время проведения ПДКТ-сканирования по-прежнему остается нерешенной проблемой. Здесь, как предполагается, методы ИИ будут дополнять стратегии, основанные на моделях. Уже сегодня 4D-ПДКТ с биннингом по фазе дыхания и коррекция движения с помощью глубокого обучения продемонстрировали снижение размытости и несоответствия изображений при свободном дыхании или неполноценной задержке дыхания, улучшая качество реконструированных изображений печени и грудной клетки без существенных изменений в процессе проведения сканирования [41, 46, 52]. Эти подходы являются естественными кандидатами для более тесной интеграции в реконструкцию, где изученные априорные данные могут упорядочить разреженные или искажённые изображения. ИИ реконструкция на основе траектории некруговых орбит, а также оптимизация и ИИ-планирование этих траекторий будет развиваться параллельно с развитием адаптированных моделей взвешивания и Z-семплирования, позволяющих дополнительно уменьшить число артефактов [38, 39, 47, 66, 87, 88]. Прогнозирование на основе глубокого машинного обучения также будет совершенствоваться, все более эффективно решая различные задачи виртуального моделирования процедур. В перспективе эти блоки ИИ будут объединены с автоматикой и робототехникой, благодаря чему слияние, управление движением и минимальное по дозе высококачественное сканирование станут обычным делом при проведении различных интервенционно-радиологических процедур [78, 89, 90].
Заключение
Следует отметить, что за 20 лет своего клинического использования ПДКТ прошла путь от «дополнительной» или «вспомогательной» мало кому известной опции до практически незаменимого комплекса технологий визуализации, планирования, навигации и оценки непосредственного ответа на лечение при проведении многих сложных рентгенохирургических вмешательств. Объединив преимущества рентгеноскопии, ЦСА и компьютерной томографии, ПДКТ предопределила создание принципиально новых алгоритмов лечения, включающих в себя единый непрерывный цикл «планирования-навигации-контроля» без логистических пауз и необходимости перемещения пациентов из рентгеноперационной в другие подразделения и обратно. Очевидными клиническими выгодами от тесной интеграции ПДКТ и ПДКТ-технологий в рабочий процесс уже сегодня являются повышение технической и клинической успешности процедур, экономия времени и контрастных препаратов, а также снижение лучевой нагрузки на пациента и персонал.
Перспективы дальнейшего развития ПДКТ-технологий связаны прежде всего с улучшением ПДКТ-визуализации с параллельным снижением лучевой нагрузки, разработкой систем синхронизации дыхания и движений пациента во время проведения вмешательств, а также с развитием роботических установок для проведения как чрескожных, так и эндоваскулярных процедур. Ангиографическая установка с возможностью выполнения ПДКТ становится таким образом «технологическим ядром» интервенционных процедур к которому, по мере развития технологий, будут интегрироваться (сопрягаться) дополнительные системы роботизированного наведения, оптического и электромагнитного слежения, ультразвуковые сканеры и другое оборудование, а также голографический интерфейс, который позволит «видеть» анатомические структуры и инструменты не только на рентгеновских мониторах, но и через очки дополненной реальности в режиме реального времени.
Таким образом уже сегодня ПДКТ стала обязательной составляющей проведения многих интервенционно-радиологических вмешательств, а в ближайшие годы эволюционирует в интеллектуальную платформу, где визуализация, планирование, навигация, лечение и оценка его эффективности сольются в единый, самонастраивающийся технологический цикл, направленный на то, чтобы выполнять рентгенохирургические вмешательства еще быстрее, точнее и безопаснее. Поэтому знание фундаментальных принципов работы ПДКТ, а также современных и доступных для клинического использования ПДКТ-технологий должно стать неотъемлемой частью подготовки врачей по специальности рентгенэндоваскулярные диагностика и лечение. Важным для России шагом в будущее является также включение ПДКТ и многочисленных ПДКТ-технологий в номенклатуру медицинских услуг и стандарты оказания медицинской помощи в области интервенционной нейрорадиологии, интервенционной онкологии и интервенционной кардиологии.
Благодарности: Авторы выражают благодарность художнику-иллюстратору Балахниной Ксении Павловне за помощь в подготовке иллюстраций.
Список литературы:
- Fahrig R., Jaffray D.A., Sechopoulos I., Stayman J.W. Flat-panel conebeam CT in the clinic: history and current state. J Med Imaging (Bellingham). 2021; 8(5): 052115. doi: 10.1117/1.JMI.8.5.052115. Epub 2021 Oct 28.
- Балахнин П.В., Багненко С.С., Беляев А.М. Плоскодетекторная компьютерная томография в интервенционной радиологии: Предпосылки появления и история создания. Медицина высоких технологий. 2024; 2(1): 12-34.
- Kalender W.A., Kyriakou Y. Flat-detector computed tomography (FD-CT). Eur Radiol. 2007; 17(11): 2767-79. doi: 10.1007/s00330-007-0651-9. Epub 2007 Jun 23.
- Gupta R., Cheung A.C., Bartling S.H., Lisauskas J., Grasruck M., Leidecker C., Schmidt B., Flohr T., Brady T.J. Flat-panel volume CT: Fundamental principles, technology, and applications. Radiographics. 2008; 28(7): 2009-22. doi: 10.1148/rg.287085004.
- Rooij W.J., Sprengers M.E., Gast A.N., Peluso J.P.P., Sluzewski M. 3D rotational angiography: the new gold standard in the detection of additional intracranial aneurysms. AJNR Am J Neuroradiol. 2008; 29(5): 976-9. doi: 10.3174/ajnr.A0964. Epub 2008 Feb 7.
- Raz E., Shapiro M., Shepherd T.M., Nossek E., Yaghi S., Gold D.M., Ishida K., Rucker J.C., Belinsky I., Kim E., Grory B.M., Mir O., Hagiwara M., Agarwal S., Young M.G., Galetta S.L., Nelson P.K. Central Retinal Artery Visualization with Cone-Beam CT Angiography. Radiology. 2022; 302(2): 419-424. doi: 10.1148/radiol.2021210520. Epub 2021 Nov 16.
- Hashimoto Y., Matsushige T., Ogawa T., Sakuragouchi H., Shimonaga K., Takahashi H., Yoshiyama M., Ono C., Sakamoto S. Impact of Cone-Beam Computed Tomography Angiography on Visualization of Sylvian Veins. World Neurosurg. 2020: 143:e206-e214. doi: 10.1016/j.wneu.2020.07.118. Epub 2020 Jul 23.
- Iwazawa J., Ohue S., Hashimoto N., Abe H., Hamuro M., Mitani T. Detection of hepatocellular carcinoma: comparison of angiographic C-arm CT and MDCT. AJR Am J Roentgenol. 2010; 195(4): 882-7. doi: 10.2214/AJR.10.4417. DOI: 10.2214/AJR.10.4417.
- Балахнин П.В., Манихас Г.М., Ханевич М.Д., Аносов Н.А., Фридман М.Х., Антимоник Н.Ю., Зорина Е.Ю., Фадеев Р.В., Юсифов С.А. Предварительные результаты применения плоскодетекторной компьютерной томографии на С-дуге на фоне капиллярной фазы артериогепатикографии (ПДКТ-АГ) для диагностики метастазов колоректального рака в печень. Диагностическая и интервенционная радиология. 2010; 4(4): 19-29.
- Balakhnin P.V., Khanevich M.D., Manikhas G.M., Anosov N.A., Zorina E.J. Chemoembolization of colorectal liver metastases: Detection and response evaluation with c-arm computed tomography. Journal of Vascular and Interventional Radiology. 2012; 23(4): 579.
- Балахнин П.В., Шмелев А.С., Шачинов Е.Г., Цикоридзе М.Ю., Поздняков А.В., Мацко Д.Е., Моисеенко В.М. Природа и перфузионная динамика перитуморального кольцевого контрастирования мелких (5-9 мм) и очень мелких (< 5 мм) гиповаскулярных метастазов в печени: Анализ данных динамической КТ-артериогепатикографии. Практическая онкология. 2017; 18(S1): 58-78.
- Racadio J.M., Babic D., Homan R., Rampton J.W., Patel M.N., Racadio J.M., Johnson N.D. Live 3D guidance in the interventional radiology suite. AJR Am J Roentgenol. 2007; 189(6): W357-64. doi: 10.2214/AJR.07.2469.
- Morimoto M., Numata K., Kondo M., Nozaki A., Hamaguchi S., Takebayashi S., Tanaka K. C-arm cone beam CT for hepatic tumor ablation under real-time 3D imaging. AJR Am J Roentgenol. 2010; 194(5): W452-4. doi: 10.2214/AJR.09.3514.
- Балахнин П.В., Шачинов Е.Г., Шмелев А.С., Мелдо А.А., Цикоридзе М.Ю., Черниковский И.Л., Егоренков В.В., Моисеенко В.М. Внутриартериальное контрастирование для визуализации, навигации, мониторинга и оценки ответа на лечение при проведении чрескожной криоабляции гиповаскулярных метастазов в печени. Практическая онкология. 2018; 19(1): 69-92.
- Balakhnin P., Shachinov E., Shmelev A. С-arm CT angiographically-assisted percutaneous cryoablation of liver metastases: Bleeding control and other benefits. Journal of Vascular and Interventional Radiology. 2021. 32: e34.
- Smits M.L.J., Bruijnen R.C.G., Tetteroo P., Vonken E-J.P.A., Meijerink M.R., Hagendoorn J., de Bruijne J., Prevoo W. Hepatic Arteriography and C-Arm CT-Guided Ablation (HepACAGA) to Improve Tumor Visualization, Navigation and Margin Confirmation in Percutaneous Liver Tumor Ablation. Cardiovasc Intervent Radiol. 2023; 46(10): 1365-1374. doi: 10.1007/s00270-023-03545-4. Epub 2023 Sep 13.
- Wijnen N., Bruijnen R.C.G., Vonken E-J.P.A., de Jong H.W.A.M., de Bruijne J., Bol G.M., Hagendoorn J., Intven M.P.W., Smits M.L.J. Conventional versus Hepatic Arteriography and C-Arm CT-Guided Ablation of Liver Tumors (HepACAGA): A Comparative Analysis. Cancers (Basel). 2024; 16(10): 1925. doi: 10.3390/cancers16101925.
- Key B.M., Tutton S.M., Scheidt M.J. Cone-Beam CT With Enhanced Needle Guidance and Augmented Fluoroscopy Overlay: Applications in Interventional Radiology. AJR Am J Roentgenol. 2023; 221 (1): 92-101. doi: 10.2214/AJR.22.28712. Epub 2023 Feb 22.
- Deschamps F., Solomon S.B., Thornton R.H., Rao P., Hakime A., Kuoch v., de Baere T. Computed analysis of three-dimensional cone-beam computed tomography angiography for determination of tumor-feeding vessels during chemoembolization of liver tumor: a pilot study. Cardiovasc Intervent Radiol. 2010; 33(6): 1235-42. doi: 10.1007/s00270-010-9846-6.
- Kim H-C. Role of C-arm cone-beam CT in chemoembolization for hepatocellular carcinoma. Korean J Radiol. 2015; 16(1): 114-24. doi: 10.3348/kjr.2015.16.1.114. Epub 2015 Jan 9.
- Tacher V., Radaelli A., Lin M., Geschwind J-F. How I do it: Cone-beam CT during transarterial chemoembolization for liver cancer. Radiology. 2015 Feb;274(2):320-34. doi: 10.1148/radiol.14131925.
- Solim L.A., Atasoy D., Vogl T.J. The efficacy of cone-beam computed tomography-guided transcatheter arterial chemoembolization in hepatocellular carcinoma survival: A systematic review. J Clin Imaging Sci. 2024: 14:25. doi: 10.25259/JCIS_32_2024. eCollection 2024.
- Bannangkoon K., Hongsakul K., Tubtawee T. Impact of cone-beam computed tomography with automated feeder detection software on the survival outcome of patients with hepatocellular carcinoma during treatment with conventional transarterial chemoembolization. BMC Gastroenterol. 2021; 21(1): 419. doi: 10.1186/s12876-021-02004-z.
- Балахнин П.В., Беляев А.М., Багненко С.С., Буровик И.А., Шмелев А.С. Технологии плоскодетекторной компьютерной томографии в интервенционной онкологии: Диагностика, стадирование и лечение гепатоцеллюлярного рака. Медицина высоких технологий. 2023; 1(1): 6-25.
- Балахнин П.В., Шачинов Е.Г., Малькевич В.И., Шмелев А.С., Курносов И.А. Выполнение трансартериальной химиоэмболизации под контролем плоскодетекторной компьютерной томографии в 3 раза улучшает 3- и 5-летнюю выживаемость пациентов с промежуточным гепатоцеллюлярным раком по сравнению с химиоэмболизацией без использования ПДКТ-технологий. Вопросы онкологии. 2025; 71(S3): 666-667.
- Denton W.D., Meredith N., Ozen M. Tracking and Navigation Technologies for Image-Guided Trans-Arterial Interventions. Tech Vasc Interv Radiol. 2024 Dec;27(4):101010. doi: 10.1016/j.tvir.2024.101010. Epub 2024 Nov 22.
- Bapst B., Lagadec M., Breguet R., Vilgrain V., Ronot M. Cone Beam Computed Tomography (CBCT) in the Field of Interventional Oncology of the Liver. Cardiovasc Intervent Radiol. 2016 Jan;39(1):8-20. doi: 10.1007/s00270-015-1180-6. Epub 2015 Jul 16.
- Raz E., Nossek E., Sahlein D.H., Sharashidze V., Narayan V., Ali A., Esparza R., Peschillo S., Chung C., Diana F., Syed S., Nelson P.K., Shapiro M. Principles, techniques and applications of high resolution cone beam CT angiography in the neuroangio suite. J Neurointerv Surg. 2023; 15(6): 600-607. doi: 10.1136/jnis-2022-018722. Epub 2022 Jul 14.
- Балахнин П.В., Буровик И.А., Багненко С.С. Технологии визуализации, наведения и слежения в интервенционной онкологии: Современные возможности и перспективы дальнейшего развития. Медицина высоких технологий. 2024; 2(2): 5-21.-EDN: CHVTFU.
- Barral M., Chevallier O., Cornelis F.H. Perspectives of Cone-beam Computed Tomography in Interventional Radiology: Techniques for Planning, Guidance, and Monitoring. Tech Vasc Interv Radiol. 2023; 26(3): 100912. doi: 10.1016/j.tvir.2023.100912. Epub 2023 Oct 20.
- Serrano E., José J.V., Páez-Carpio A., Matute-González M., Werner M.F., López-Rueda A. Cone Beam computed tomography (CBCT) applications in image-guided minimally invasive procedures. Radiologia (Engl Ed). 2025; 67(1): 38-53. doi: 10.1016/j.rxeng.2023.09.009. Epub 2025 Feb 1.
- Zhong B-Y., Jia Z-Z., Zhang W., Liu C., Ying S-H., Yan Z-P., Ni C-F., Clinical Guidelines Committee Of Chinese College Of Interventionalists. Application of Cone-beam Computed Tomography in Interventional Therapies for Liver Malignancy: A Consensus Statement by the Chinese College of Interventionalists. J Clin Transl Hepatol. 2024; 12(10): 886-891. doi: 10.14218/JCTH.2024.00213. Epub 2024 Sep 12.
- Бредер В.В., Базин И.С., Балахнин П.В., Виршке Э.Р., Косырев В.Ю., Ледин Е.В., Медведева Б.М., Моисеенко Ф.В., Мороз Е.А., Петкау В.В., Покатаев И.А. Злокачественные опухоли печени и желчевыводящей системы. Злокачественные опухоли. 2023; 13(3S2-1): 494-538.
- Долгушин Б.И., Таразов П.Г., Погребняков И.В., Тарханов А.А., Виршке Э.Р., Балахнин П.В., Поликарпов А.А. Стандарты проведения процедуры трансартериальной химиоэмболизации при лечении пациентов с гепатоцеллюлярной карциномой. Учебно-методическое пособие / Москва, 2024.
- Strobel N., Meissner O., Boese J., Brunner T., Heigl B., Hoheisel M., Lauritsch G., Nagel M., Pfister M., Rührnschopf E-P., Scholz B., Schreiber B., Spahn M., Zellerhoff M., Klingenbeck-Regn K. "3D imaging with flat-detector C-arm systems" Multislice CT. Berlin, Heidelberg: Springer Berlin Heidelberg, 2009. 33-51.
- Kyriakou Y., Struffert T., Dörfler A., Kalender W.A. Basic principles of flat detector computed tomography (FD-CT). Radiologe. 2009; 49(9): 811-9. doi: 10.1007/s00117-009-1860-9 [In German].
- Orth R.C., Wallace M.J., Kuo M.D.; Technology Assessment Committee of the Society of Interventional Radiology. C-arm cone-beam CT: general principles and technical considerations for use in interventional radiology. J Vasc Interv Radiol. 2008 Jun;19(6): 814-20. doi: 10.1016/j.jvir.2008.02.002. Epub 2008 Apr 23.
- Schernthaner R.E., Chapiro J., Sahu S., Withagen P., Duran R., Sohn J.H., Radaelli A., van der Bom I.M., Geschwind J-F.H., Lin M. Feasibility of a Modified Cone-Beam CT Rotation Trajectory to Improve Liver Periphery Visualization during Transarterial Chemoembolization. Radiology. 2015; 277(3): 833-41. doi: 10.1148/radiol.2015142821. Epub 2015 May 20.
- Petroulia V.D., Kaesmacher J., Piechowiak E.I., Dobrocky T., Pilgram-Pastor S.M., Gralla J., Wagner F., Mordasini P. Evaluation of Sine Spin flat detector CT imaging compared with multidetector CT. J Neurointerv Surg. 2023; 15(3): 292-297. doi: 10.1136/neurintsurg-2021-018312. Epub 2022 Mar 22.
- Tang X., Krupinski E.A., Xie H., Stillman A.E. On the data acquisition, image reconstruction, cone beam artifacts, and their suppression in axial MDCT and CBCT - A review. Med Phys. 2018 Jul 17. doi: 10.1002/mp.13095. Online ahead of print.
- Burgio M.D., Benseghir T., Roche V., Alba C.G., Debry J.B., Sibert A., Vilgrain V., Ronot M. Clinical impact of a new cone beam CT angiography respiratory motion artifact reduction algorithm during hepatic intra-arterial interventions. Eur Radiol. 2020; 30(1): 163-174. doi: 10.1007/s00330-019-06355-w. Epub 2019 Jul 29.
- Fahrig R., Dixon R., Payne T., Morin R.L., Ganguly A., Strobel N. Dose and image quality for a cone-beam C-arm CT system. Med Phys. 2006; 33(12): 4541-50. doi: 10.1118/1.2370508.
- Gosch D., Kurze W., Deckert F., Schulz T., Patz A., Kahn T. Radiation exposure with 3D rotational angiography of the skull. Rofo. 2006; 178(9): 880-5. doi: 10.1055/s-2006-926955 [In Germ].
- Guberina N., Lechel U., Forsting M., Mönninghoff C., Dietrich U., Ringelstein A. Dose comparison of classical 2-plane DSA and 3D rotational angiography for the assessment of intracranial aneurysms. Neuroradiology. 2016; 58(7): 673-8. doi: 10.1007/s00234-016-1671-4. Epub 2016 Mar 12.
- Kim S., Yoshizumi T.T., Toncheva G., Yoo S., Yin F-F. Comparison of radiation doses between cone beam CT and multi detector CT: TLD measurements. Radiat Prot Dosimetry. 2008; 132(3): 339-45. doi: 10.1093/rpd/ncn305. Epub 2008 Dec 13.
- Jung Y., Lee H., Jun H., Cho S. Evaluation of Motion Artifact Correction Technique for Cone-Beam Computed Tomography Image Considering Blood Vessel Geometry. J Clin Med. 2024; 13(8): 2253. doi: 10.3390/jcm13082253.
- Hatamikia S., Biguri A., Herl G., Kronreif G., Reynolds T., Kettenbach J., Russ T., Tersol A., Maier A., Figl M., Siewerdsen J.H., Birkfellner W. Source-detector trajectory optimization in cone-beam computed tomography: a comprehensive review on today's state-of-the-art. Phys Med Biol. 2022; 67(16). doi: 10.1088/1361-6560/ac8590.
- Miyayama S., Yamashiro M., Nagai K., Yokka A., Yoshida M., Sakuragawa N. Performance of novel virtual parenchymal perfusion software visualizing embolized areas of transcatheter arterial chemoembolization for hepatocellular carcinoma. Hepatol Res. 2017; 47(5): 446-454. doi: 10.1111/hepr.12766. Epub 2016 Aug 11.
- Derbel H., Kobeiter H., Pizaine G., Ridouani F., Luciani A., Radaelli A., Van der Sterren W., Chiaradia M., Tacher V. Accuracy of a Cone-Beam CT Virtual Parenchymal Perfusion Algorithm for Liver Cancer Targeting during Intra-arterial Therapy. J Vasc Interv Radiol. 2018; 29(2): 254-261.e2. doi: 10.1016/j.jvir.2017.08.023. Epub 2017 Nov 28.
- Brendlin A.S., Estler A., Plajer D., Lutz A., Grözinger G., Bongers M.N., Tsiflikas I., Afat S., Artzner C.P. AI Denoising Significantly Enhances Image Quality and Diagnostic Confidence in Interventional Cone-Beam Computed Tomography. Tomography. 2022; 8(2): 933-947. doi: 10.3390/tomography8020075.
- Schulze R., Heil U., Gross D., Bruellmann D.D., Dranischnikow E., Schwanecke U., Schoemer E. Artefacts in CBCT: a review. Dentomaxillofac Radiol. 2011; 40(5): 265-73. doi: 10.1259/dmfr/30642039.
- Reynolds T., Dillon O., Ma Y., Hindley N., Stayman J.W., Bazalova-Carter M. Investigating 4D respiratory cone-beam CT imaging for thoracic interventions on robotic C-arm systems: a deformable phantom study. Phys Eng Sci Med. 2024; 47(4): 1751-1762. doi: 10.1007/s13246-024-01491-0. Epub 2024 Oct 24.
- Cancelliere N.M., Hummel E., van Nijnatten F., van de Haar P., Withagen P., van Vlimmeren M., Hallacoglu B., Agid R., Nicholson P., Pereira V.M. The butterfly effect: improving brain cone-beam CT image artifacts for stroke assessment using a novel dual-axis trajectory. J Neurointerv Surg. 2023; 15(3): 283-287. doi: 10.1136/neurintsurg-2021-018553. Epub 2022 Apr 27.
- Tovar-Arriaga S., Tita R., Pedraza-Ortega J.C., Gorrostieta E., Kalender W.A. Development of a robotic FD-CT-guided navigation system for needle placement-preliminary accuracy tests. Int J Med Robot. 2011; 7(2): 225-36. doi: 10.1002/rcs.393. Epub 2011 Apr 28.
- Stayman J.W., Capostagno S., Gang G.J., Siewerdsen J.H. Task-driven source-detector trajectories in cone-beam computed tomography: I. Theory and methods. J Med Imaging (Bellingham). 2019; 6(2): 025002. doi: 10.1117/1.JMI.6.2.025002. Epub 2019 May 2.
- Capostagno S., Stayman J.W., Jacobson M., Ehtiati T., Weiss C.R., Siewerdsen J.H. Task-driven source-detector trajectories in cone-beam computed tomography: II. Application to neuroradiology. J Med Imaging (Bellingham). 2019; 6(2): 025004. doi: 10.1117/1.JMI.6.2.025004. Epub 2019 May 9.
- Miller D.L., Vañó E., Bartal G., Balter S., Dixon R., Padovani R., Schueler B., Cardella J.F., de Baère T.; Cardiovscular and Interventional Radiology Society of Europe; Society of Interventional Radiology. Occupational radiation protection in interventional radiology: a joint guideline of the Cardiovascular and Interventional Radiology Society of Europe and the Society of Interventional Radiology. Cardiovasc Intervent Radiol. 2010; 33(2): 230-9. doi: 10.1007/s00270-009-9756-7. Epub 2009 Dec 18.
- Garg T., Shrigiriwar A. Radiation Protection in Interventional Radiology. Indian J Radiol Imaging. 2022; 31(4): 939-945. doi: 10.1055/s-0041-1741049. eCollection 2021 Oct.
- Loffroy R., Lin m. Yenokyan G., Rao P.P., Bhagat N., Noordhoek N., Radaelli A., Blijd J., Liapi E., Geschwind J-F. Intraprocedural C-arm dual-phase cone-beam CT: can it be used to predict short-term response to TACE with drug-eluting beads in patients with hepatocellular carcinoma? Radiology. 2013; 266(2): 636-48. doi: 10.1148/radiol.12112316. Epub 2012 Nov 9.
- Barral M., Lassalle L., Gardavaud F., Lehrer R., Haffaf I., Agbonon R., Cussenot O., Cornelis F.H. Virtual Injection Software Reduces Radiation Exposure and Procedural Time of Prostatic Artery Embolization Performed with Cone-Beam CT. J Vasc Interv Radiol. 2024; 35(3): 409-415. doi: 10.1016/j.jvir.2023.11.012. Epub 2023 Nov 25.
- Li M., Qu W., Zhang D., Zhong B., Li Z., Jiang Z., Ni G., Ni C. Evaluation of Radiation Exposure and Influential Factors in Cone-Beam Computed Tomography (CBCT) of the Head and Abdomen during Interventional Procedures. Tomography. 2024; 10(3): 320-330. doi: 10.3390/tomography10030025.
- Becker H-C., Meissner O., Waggershauser T. C-arm CT-guided 3D navigation of percutaneous interventions. Radiologe. 2009; 49(9): 852-5. doi: 10.1007/s00117-009-1866-3 [In Germ]
- Treb K., Ji X., Feng M., Zhang R., Periyasamy S., Laeseke P.F., Dingle A.M., Brace C.L., Li K. A C-arm photon counting CT prototype with volumetric coverage using multi-sweep step-and-shoot acquisitions. Phys Med Biol. 2022; 67(21): 10.1088/1361-6560/ac950d. doi: 10.1088/1361-6560/ac950d.
- Choo J.Y., Park C.M., Lee N.K., Lee S.M., Lee H-J., Goo J.M. Percutaneous transthoracic needle biopsy of small (≤ 1 cm) lung nodules under C-arm cone-beam CT virtual navigation guidance. Eur Radiol. 2013; 23(3): 712-9. doi: 10.1007/s00330-012-2644-6. Epub 2012 Sep 14.
- Курносов И.А., Балахнин П.В., Гуляев Д.А., Субботина Д.Р., Малькевич В.И., Муравцева А.Л., Шмелев А.С., Чиркин В.Ю., Буровик И.А., Багненко С.С., Беляев А.М. Плоскодетекторная компьютерная томография: новые возможности нейронавигации в режиме реального времени при проведении стереотаксической биопсии новообразований головного мозга. Вопросы онкологии. 2025; 71(6): 00-00.-DOI: 10.37469/0507-3758-2025-71-6-OF-2310. Опубликована 01.12.2025.
- Braak S.J., van Strijen M.J.L., van Leersum M., van Es H.W., van Heesewijk J.P.M. Real-Time 3D fluoroscopy guidance during needle interventions: technique, accuracy, and feasibility. AJR Am J Roentgenol. 2010; 194(5): W445-51. doi: 10.2214/AJR.09.3647.
- Chehab M., Kouri B.E., Miller M.J., Venkatesan A.M. Image Fusion Technology in Interventional Radiology. Tech Vasc Interv Radiol. 2023; 26(3): 100915. doi: 10.1016/j.tvir.2023.100915. Epub 2023 Oct 21.
- Busser W.M.H., Braak S.J., Fütterer J.J., van Strijen M.J.L., Hoogeveen Y.L., de Lange F., Schultze Kool L.J. Cone beam CT guidance provides superior accuracy for complex needle paths compared with CT guidance. Br J Radiol. 2013; 86(1030): 20130310. doi: 10.1259/bjr.20130310. Epub 2013 Aug 2.
- Cazzato R.L., Battistuzzi J-B., Catena V., Grasso R.F., Zobel B.B., Schena E., Buy X., Palussiere J. Cone-Beam Computed Tomography (CBCT) Versus CT in Lung Ablation Procedure: Which is Faster? Cardiovasc Intervent Radiol. 2015; 38(5): 1231-6. doi: 10.1007/s00270-015-1078-3. Epub 2015 Mar 19.
- Abi-Jaoudeh N., Fisher T., Jacobus J., Skopec M., Radaelli A., Van Der Bom I.M., Wesley R., Wood B.J. Prospective Randomized Trial for Image-Guided Biopsy Using Cone-Beam CT Navigation Compared with Conventional CT. J Vasc Interv Radiol. 2016; 27(9): 1342-1349. doi: 10.1016/j.jvir.2016.05.034. Epub 2016 Jul 25.
- Braak S.J., van Strijen M.J.L., van Es H.W., Nievelstein R.A.J., van Heesewijk J.P.M. Effective dose during needle interventions: cone-beam CT guidance compared with conventional CT guidance. J Vasc Interv Radiol. 2011; 22(4): 455-61. doi: 10.1016/j.jvir.2011.02.011.
- Durack J.C., Brown K.T., Avignon G., Brody L.A., Sofocleous C.T., Erinjeri J.P., Solomon S.B. Assessment of automated cone-beam CT vessel identification software during transarterial hepatic embolisation: radiation dose, contrast medium volume, processing time, and operator perspectives compared to digital subtraction angiography. Clin Radiol. 2018; 73(12): 1057.e1-1057.e6. doi: 10.1016/j.crad.2018.08.005. Epub 2018 Sep 13.
- Cui Z., Shukla P.A., Habibollahi P., Park H.S., Fischman A., Kolber M.K. A systematic review of automated feeder detection software for locoregional treatment of hepatic tumors. Diagn Interv Imaging. 2020; 101(7-8): 439-449. doi: 10.1016/j.diii.2020.01.011. Epub 2020 Feb 5.
- Hohenforst-Schmidt W., Zarogoulidis P., Vogl T., Turner J.F., Browning R., Linsmeier B., Huang H., Li Q., Darwiche K., Freitag L., Simoff M., Kioumis I., Zarogoulidis K., Brachmann J. Cone Beam Computertomography (CBCT) in Interventional Chest Medicine - High Feasibility for Endobronchial Realtime Navigation. J Cancer. 2014; 5(3): 231-41. doi: 10.7150/jca.8834. eCollection 2014.
- de Ruiter Q.M.B., Karanian J.W., Bakhutashvili I., Esparza-Trujillo J.A., Varble N.A., van der Sterren W., Schampaert S., van der Bom I.M.J., Li X., Mauda-Havakuk M., Fontana J.R., Pritchard W.F., Wood B.J. Endobronchial Navigation Guided by Cone-Beam CT-Based Augmented Fluoroscopy without a Bronchoscope: Feasibility Study in Phantom and Swine. J Vasc Interv Radiol. 2020; 31(12): 2122-2131. doi: 10.1016/j.jvir.2020.04.036. Epub 2020 Oct 2.
- Ghosn M., Elsakka A.S., Ridouani F., Doustaly R., Mingione L., Royalty K., Ziv E., Alexander E., Maxwell A., Monette S., Kim H.S., Short R.F., Tam A.L., Suh R.D., Solomon S.B. Augmented fluoroscopy guided transbronchial pulmonary microwave ablation using a steerable sheath. Transl Lung Cancer Res. 2022; 11(2): 150-164. doi: 10.21037/tlcr-21-864.
- Ridouani F., Ghosn M., Doustaly R., Gonzalez-Aguirre A.J., Ziv E., Solomon S.B., Edward Boas F., Yarmohammadi H. Accuracy of a CBCT-based virtual injection software for vessel detection during hepatic arterial embolization. Eur J Radiol. 2022; 150: 110273. doi: 10.1016/j.ejrad.2022.110273. Epub 2022 Mar 21.
- Brock K.K., Chen S.R., Sheth R.A., Siewerdsen J.H. Imaging in Interventional Radiology: 2043 and Beyond. Radiology. 2023; 308(1): e230146. doi: 10.1148/radiol.230146.
- Sutter O., Fihri A., Ourabia-Belkacem R., Sellier N., Diallo A., Seror O. Real-Time 3D Virtual Target Fluoroscopic Display for Challenging Hepatocellular Carcinoma Ablations Using Cone Beam CT. Technol Cancer Res Treat. 2018; 17: 1533033818789634. doi: 10.1177/1533033818789634.
- Arrichiello A., Ierardi A.M., Caruso A., Grillo P., Di Meglio L., Biondetti P., Iavarone M., Sangiovanni A., Angileri S.A., Floridi C., Wood B., Carrafiello G. Virtual Treatment Zone From Cone Beam CT Commonly Alters Treatment Plan and Identifies Tumor at Risk for Under-Treatment in US or US Fusion-Guided Microwave Ablation of Liver Tumors. Technol Cancer Res Treat. 2023; 22:15330338231181284. doi: 10.1177/15330338231181284.
- Biondetti P., Ierardi A.M., Casiraghi E., Caruso A., Grillo P., Carriero S., Lanza C., Angileri S.A., Sangiovanni A., Iavarone M., Guzzardi G., Carrafiello G. Clinical Impact of a Protocol Involving Cone-Beam CT (CBCT), Fusion Imaging and Ablation Volume Prediction in Percutaneous Image-Guided Microwave Ablation in Patients with Hepatocellular Carcinoma Unsuitable for Standard Ultrasound (US) Guidance. J Clin Med. 2023; 12(24): 7598. doi: 10.3390/jcm12247598.
- Pionteck A., Pierrat B., Gorges S., Albertini J.N., Avril S. Evaluation and Verification of Fast Computational Simulations of Stent-Graft Deployment in Endovascular Aneurysmal Repair. Front Med Technol. 2021; 3:704806. doi: 10.3389/fmedt.2021.704806.
- Sheth N.M., Zbijewski W., Jacobson M.W., Abiola G., Kleinszig G., Vogt S., Soellradl S., Bialkowski J., Anderson W.S., Weiss C.R., Osgood G.M., Siewerdsen J.H. Mobile C-Arm with a CMOS detector: Technical assessment of fluoroscopy and Cone-Beam CT imaging performance. Med Phys. 2018; 45(12): 5420-5436. doi: 10.1002/mp.13244.
- Shi L., Lu M., Bennett N.R., Shapiro E., Zhang J., Colbeth R., Star-Lack J., Wang A.S. Characterization and potential applications of a dual-layer flat-panel detector. Med Phys. 2020; 47(8): 3332-3343. doi: 10.1002/mp.14211. Epub 2020 May 18.
- Stahl F., Schafer D., Omar A., van de Haar P., van Nijnatten F., Withagen P., Thran A., Hummel E., Menser B., Holmberg A., Soderman M., Falk Delgado A., Poludniowski G. Performance characterization of a prototype dual-layer cone-beam computed tomography system. Med Phys. 2021; 48(11):6740-6754. doi: 10.1002/mp.15240.
- Müller K., Datta S., Ahmad M., Choi J.H., Moore T., Pung L., Niebler C., Gold G.E., Maier A., Fahrig R. Interventional dual-energy imaging-Feasibility of rapid kV-switching on a C-arm CT system. Med Phys. 2016; 43(10): 5537. doi: 10.1118/1.4962929.
- Gurgitano M., Angileri S.A., Rodà G.M., Liguori A., Pandolfi M., Ierardi A.M., Wood B.J., Carrafiello G. Interventional Radiology ex-machina: impact of Artificial Intelligence on practice. Radiol Med. 2021 Jul;126(7):998-1006. doi: 10.1007/s11547-021-01351-x. Epub 2021 Apr 16.
- Glielmo P., Fusco S., Gitto S., Zantonelli G., Albano D., Messina C., Sconfienza L.M., Mauri G. Artificial intelligence in interventional radiology: state of the art. Eur Radiol Exp. 2024; 8(1): 62. doi: 10.1186/s41747-024-00452-2.
- Lanza C., Carriero S., Buijs E.F.M., Mortellaro S., Pizzi C., Sciacqua L.V., Biondetti P., Angileri S.A., Ianniello A.A., Ierardi A.M., Carrafiello G. Robotics in Interventional Radiology: Review of Current and Future Applications. Technol Cancer Res Treat. 2023; 22:15330338231152084. doi: 10.1177/15330338231152084.
- Li F., Bi Y., Huang D., Jiang Z., Navab N. Robotic CBCT meets robotic ultrasound. Int J Comput Assist Radiol Surg. 2025 Jun;20(6):1049-1057. doi: 10.1007/s11548-025-03336-x. Epub 2025 Mar 12.
Если вы хотите узнать побольше о бесплатных возможностях ФБГУ НМИЦ онкологии им. Н.Н. Петрова Минздрава России, получить очную или заочную консультацию по диагностике и лечению, записаться на приём, ознакомьтесь с информацией на странице.
Если вы хотите общаться с нами через социальные сети, обратите внимание на аккаунты в ВКонтакте и Telegram.
- Плоскодетекторная компьютерная томография в интервенционной радиологии: фундаментальные принципы, современные технологии и перспективы дальнейшего развития
- Может ли экстракорпоральное оплодотворение спровоцировать рак?
- Внутрибольничная пневмония: диагностика, лечение и профилактика
- Рак и наследственность
- Профессор Светлана Кулева: «До сих просыпаюсь от страха, что иду на экзамен по взрослой хирургии»